
����Ŀ�����÷ϼ���(��Ҫ�ɷ�ΪNa2CO3)�������᳧β���е�SO2�����Ƶ���ˮNa2SO3(��Ʒ������������ͼ��ʾ��
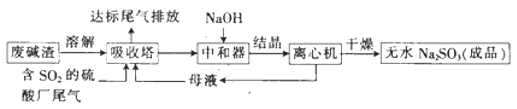
(1)ij���᳧�ŷų���β����SO2�ĺ����ر��{�����ϼ����������㣬��ʱ�����������ڷ�����Ӧ�����ӷ���ʽΪ_______________(������H2O��SO2��Ӧ)��
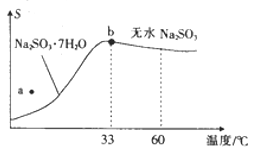
(2)�������Ƶ��ܽ��������ͼ��ʾ�����������������ᾧ���ķ�����___________(���������ᾧ���������½ᾧ��)��ͼ��a����ʾ��ɢϵ���Ϊ____________(������Һ����������������Һ������
(3)����BaCl2��H2O2����ϡ����Ļ����Һ���Լ������Ʒ���е�SO32-��ԭ��������Ʒ���к���ij�����������ӡ�
�ٸ�����������Ϊ________________(�����ӷ��ţ���
��25��ʱ�����ֱ��ε�Ksp���±���ʾ��
��ѧʽ | BaSO4 | BaSO3 |
Ksp | 1.1��10-10 | 5.5��10-7 |
���õ�������Ʒ������ˮ�������Һ��SO32-��Ũ��Ϊ0.5mol L-1��Ϊ����������Ũ�ȵ�10���������Һ�м���������0.5mol��L-1��BaCl2��Һ����ַ�Ӧ��c(Ba2+)=_______mol L-1�������ʱ��Һ����ı仯���Բ��ƣ�
(4)ijͬѧ�������·�������SO32-��
![]()
��ϴ��ʱʹ�õ��Լ����Ϊ____________(����ĸ)��
a.ϡHNO3 b.����ˮ c.ϡH2SO4
�ڸ������������е�����(w��x��y)_____________ (������������������)�������Ʒ������SO32-�İٷֺ��������ܣ���SO32-�İٷֺ���Ϊ (�����ܣ���˿ղ���)�������ܣ���������_____________(���ܣ���˿ղ����
���𰸡� CO32-+2SO2+H2O=CO2+2HSO3- �����ᾧ ��Һ SO42- 2.2��10-5 b ���� ��ɫ����B���������ᷴӦʱ��BaSO3û��ȫ���ܽ�
��������������Ҫ������Ļ������������Ƶ����ʵ����ʡ�
(1)ij���᳧�ŷų���β����SO2�ĺ����ر��{�����ϼ����������㣬��ʱ�����������ڷ�����Ӧ�������������ƺͶ�����̼����Ӧ�����ӷ���ʽΪCO32-+2SO2+H2O=CO2+2HSO3-��
(2)�������������ᾧ���õ���ˮNa2SO3����ˮNa2SO3���ܽ�����¶����߱仯�������������ᾧ���ķ����������ᾧ��ͼ��a�㱥����Һ�к��о��壬����ͼ��a����ʾ��ɢϵ���Ϊ��Һ��
(3)�ٸ�����������Ϊ����ͨ��H2O2��SO32-��Ӧ���ɵ�SO42-��
�ڴӱ��ε�Ksp����Һ��SO32-��Ũ��ΪSO42-��10���жϣ����������ᱵ�����������������ᱵ������ʣ��SO32-��Ũ��Ϊ0.025mol L-1��c(Ba2+)=Ksp(BaSO3)/ʣ��SO32-��Ũ��=2.2��10-5mol L-1��
(4)��a.ϡHNO3�ɽ�BaSO3����ΪBaSO4��b.����ˮ��ϴȥ�������ӣ�c.ϡH2SO4�ɽ���������BaCl2ת��ΪBaSO4����ѡb��
�ڸ������������е�����(w��x��y)���ܼ������Ʒ������SO32-�İٷֺ����������ǰ�ɫ����B���������ᷴӦʱ��BaSO3û��ȫ���ܽ⡣


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ơ���������1mol�ֱ�Ͷ�뵽�������ͬŨ�ȵ������У������������������ͬ�����£� ��
A.�ƿ������
B.����������һ����
C.��һ�����
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.NaOH��Ħ������Ϊ40 g
B.1 mol O2��������������Է����������
C.1 mol OH��������Ϊ17 gmol��1
D.������Ħ����������λgmol��1������ֵ�ϵ����������ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H2FeCO4)��һ�ֶ�ܡ���Ч����������ɫˮ��������Ͷ��ˮ�л�Ѹ�ٷ�����Ӧ��
(1)Na2FeO4��Fe�Ļ��ϼ�Ϊ______________________��.
(2)��֪�������¸�����Ϊ�Ϻ�ɫ���壬��H2FeO4Ͷ��ˮ�У����������ɣ�ͬʱ�к��ɫ������������H2FeO4��ˮ��Ӧ�Ļ�ѧ����ʽΪ__________________��
(3)�ڹ�ҵ���Ʊ�Na2FeO4�ķ����ж��֡�
��.�ɷ��Ʊ��ķ�Ӧԭ�����£�
2FeSO4+6Na2O2=aNa2FeO4+M��+2Na2O+2Na2SO4
��a=_____________��
��ÿ����1mol M���÷�Ӧת�Ƶ��ӵ����ʵ���Ϊ_________mol��
��.ʪ���Ʊ��Ĺ����������£�
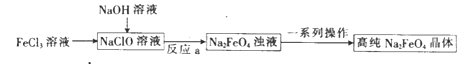
��֪��Na2FeO4��ǿ������Һ�е��ܽ�Ƚ�С��
�۷�Ӧa�У����������Na2FeO4�⣬��һ���εĻ�ѧʽΪ _____________��
��һϵ�в����������ˡ�___________��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ����������֪ʶ����ȷ����
���ʼ��仯 | ���� | ���֪ʶ | |
A | �⻯����Һ�ε�����Ƭ�� | ����ɫ | ����Ƭ������ |
B | ú������ | ��ѧ�仯 | ��Ҫ��Ӧ��̼��ˮ����ˮú���� |
C | ��ϩ�ͱ� | ����ʹ��ˮ��ɫ | �����к�����ͬ��̼̼˫�� |
D | ���Ǻ���ѿ�� | ���� | ����Ϊͬ���칹�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ƿ�ӦCO��g��+2H2��g���TCH3OH��g�����й����е������仯���ߣ��������˵����ȷ���ǣ� �� 
A.�÷�Ӧ�����ȷ�Ӧ
B.ʹ�ô�����Ӧ�ȼ�С
C.�Ȼ�ѧ����ʽΪCO��g��+2H2��g���TCH3OH��g����H=��510 kJmol��1
D.����a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��ѧ�С�����о���ѧϰ��̽�������Ƿ��ӵ���ɺͽṹʱ��Ʋ���ɵ�һ��ʵ�飺����������Һ��ֱ�ȡ2 mL�Ⱥ�ӵ�2 mL������Cu(OH)2�У������ʵ�������¼�����
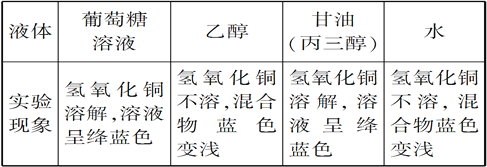
��������ʵ�鼰�����ܹ��ó�����ȷ������(����)
A. �����Ƿ����п��ܺ���ȩ��
B. �����Ƿ����п��ܺ��ж���ǻ�
C. �����ǵķ���ʽΪC6H12O6
D. �����Ƿ���̼���ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦN2��g��+3H2��g��2NH3��g����H��0�������о�Ŀ�ĺ�ʾ��ͼ������ǣ� ��
A | B | C | D | |
�о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�죨P2��P1�� | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ����N2�Է�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
ͼʾ |
|
|
|
|
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ŵ�����ʪ����ͭ�ļ��ء����������Ϊͭ������ӦΪFe+CuSO4==FeSO4+Cu���йظ÷�Ӧ��˵����ȷ���� �� ��
A. Fe�������� B. CuSO4�ǻ�ԭ��
C. Fe������ D. CuSO4����������Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com