
| ||
| ||


科目:高中化学 来源: 题型:
| A、2Na2O2+2H2O=4NaOH+O2↑ |
| B、2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
| C、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
| D、2NH3+H2SO4=(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
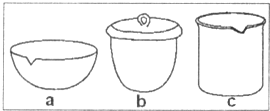
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70℃ | 57.6℃ |
| TiCl4 | -25℃ | 136.5℃ |
- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
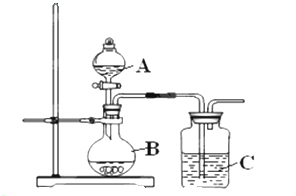 Ⅰ、某同学想通过下列实验装置来验证硫、碳、硅的非金属性的强弱,则A中的药品是
Ⅰ、某同学想通过下列实验装置来验证硫、碳、硅的非金属性的强弱,则A中的药品是| 实验序号 | 温度 | H2O2溶液初始浓度 | MnO2颗粒大小 |
| 1 | 25℃ | 4% | 无MnO2 |
| 2 | 25℃ | 12% | 1g细颗粒MnO2 |
| 3 | 25℃ | 4% | 1g细颗粒MnO2 |
| 4 | 25℃ | 4% | 1g粗颗粒MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
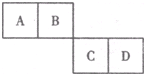 已知A、B、C、D四种短周期元素在元素周期表中的相对位置如图所示,它们的原子序数之和为46.请填空:
已知A、B、C、D四种短周期元素在元素周期表中的相对位置如图所示,它们的原子序数之和为46.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
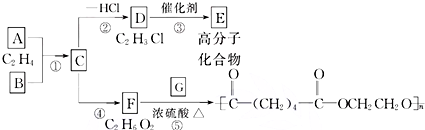
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
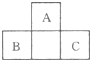 如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则:
如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com