
【题目】某兴趣小组模拟工业制漂白粉,设计了下列图的实验装置。已知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
回答下列问题:

(1)甲装置中仪器a的名称是_____________________。
(2)装置乙中饱和食盐水的作用是_____________________。
(3)①制取漂白粉的化学方程式是______________________________。
②该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],则产物中还混杂有物质的化学式是______。
③为提高Ca(ClO)2的含量,,可采取的措施是__________________(任写一种即可)。
(4)漂白粉应密封保存,原因是______________(用化学方程式表示)。
(5)家庭中常用84 消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)清洁卫生。两者同时混合使用会产生有毒的氯气,写出该反应的离子方程式________________________________。
(6)实验室用MnO2跟浓盐酸反应时,当盐酸浓度低于8mol/L时就不能生成氯气。某兴趣小组在圆底烧瓶中实际加入了MnO28.7g,20mL36.5%的浓盐酸(密度1.18g/mL),充分反应后最多能够收集到_______L标准状况下的氯气(保留3位有效数字,不考虑反应过程中溶液体积变化)。
【答案】 分液漏斗 除去氯气中混有的氯化氢 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO3)2 将丙装置浸在盛有冷水的水槽中或控制氯气产生速率(其它合理答案也给分) Ca(ClO)2+CO2+H2O=CaCO3+2HClO ClO-+Cl-+2H+=Cl2↑+H2O 0.426
【解析】(1)甲装置中仪器a具有球形特征,有玻璃活塞,在该实验中,可以控制加入的浓盐酸,为分液漏斗。(2)浓盐酸和二氧化锰反应过程中会挥发出氯化氢气体,氯化氢在氯化钠饱和溶液中易溶,而氯气难溶,通过饱和食盐水的作用是除去Cl2中混有的HCl气体。(3)①制取漂白粉的化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。②氯气和碱反应会放出热量,导致温度升高,当温度低时,氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水;当温度高时,发生了副反应:6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O,所以制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],即还混杂有物质的化学式是Ca(ClO3)2。③温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,用冰水或冷水冷却,或控制氯气产生速率,通过控制反应速率,避免反应放热瞬时温度升高。(4)漂白粉有效成分为次氯酸钙,HClO虽是强氧化性的酸,但它是比碳酸还弱的酸,受空气中的水、CO2作用而导致变质,生成CaCO3和HClO,该反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3+2HClO,所以漂白粉应密封保存。(5)NaClO与盐酸同时混合使用会产生有毒的氯气,该反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O。(6)浓盐酸的浓度是
5CaCl2+Ca(ClO3)2+6H2O,所以制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],即还混杂有物质的化学式是Ca(ClO3)2。③温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,用冰水或冷水冷却,或控制氯气产生速率,通过控制反应速率,避免反应放热瞬时温度升高。(4)漂白粉有效成分为次氯酸钙,HClO虽是强氧化性的酸,但它是比碳酸还弱的酸,受空气中的水、CO2作用而导致变质,生成CaCO3和HClO,该反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3+2HClO,所以漂白粉应密封保存。(5)NaClO与盐酸同时混合使用会产生有毒的氯气,该反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O。(6)浓盐酸的浓度是![]() ,当盐酸浓度低于8mol/L时就不能生成氯气,所以实际参加反应的氯化氢是0.02L×(11.8mol/L-8mol/L)=0.076mol。二氧化锰的物质的量是0.1mol,根据方程式MnO2+4HCl(浓)
,当盐酸浓度低于8mol/L时就不能生成氯气,所以实际参加反应的氯化氢是0.02L×(11.8mol/L-8mol/L)=0.076mol。二氧化锰的物质的量是0.1mol,根据方程式MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O可知二氧化锰过量,生成氯气的物质的量是0.076mol÷4=0.019mol,在标准状况下的体积是0.019mol×22.4L/mol=0.426L。
MnCl2+Cl2↑+2H2O可知二氧化锰过量,生成氯气的物质的量是0.076mol÷4=0.019mol,在标准状况下的体积是0.019mol×22.4L/mol=0.426L。


科目:高中化学 来源: 题型:
【题目】为了测定酸碱反应的中和反应反应热,计算时至少需要的数据是( ) ①酸的浓度和体积
②碱的浓度和体积
③比热容
④反应后溶液的质量
⑤生成水的物质的量
⑥反应前后溶液温度变化
⑦操作所需的时间.
A.①②③⑥
B.①③④⑥
C.③④⑤⑥
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由物质a为原料,制备物质d (金刚烷)的合成路线如下图所示: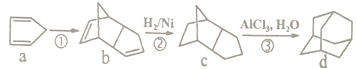
关于以上有机物说法中错误的是( )
A.物质a的分子式为C5H6
B.物质b使酸性高锰酸钾溶液和溴水褪色的原理相同
C.物质c与物质d互为同分异构体
D.物质d的一氯代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。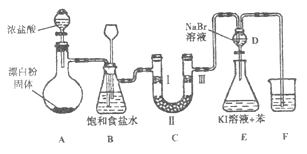
(1)装置A是氯气的发生装置,请写出该反应相应的化学方程式:。
(2)装置B中饱和食盐水的作用是;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ处依次放入物质的组合应是(填字母编号)。
编号 | I | Ⅱ | Ⅲ |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 , 该现象(填“能”或“不能”) 说明溴单质的氧化性强于碘,原因是。
(5)装置F的烧杯中的溶液不能选用下列中的(填字母编号)。a.饱和NaOH溶液 b.饱和Ca(OH)2溶液 c.饱和Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:

请回答下列问题:
(1)向操作①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有______(填离子符号)。
(2)操作②中反应的离子方程式:__________________________________。
(3)操作③中反应的离子方程式:__________________________________。
(4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)某温度下,在Ca(OH)2(Ksp=5.5×10﹣6)、Mg(OH)2(Ksp=3.2×10﹣11)、AgCl(Ksp=1.8×10﹣10)三种物质中,溶解度最小的是
(2)在粗制CuSO45H2O晶体中常含有杂质Fe2+ . 在提纯时为了除去Fe2+ , 常加入氧化剂,使Fe2+氧化为Fe3+ , 下列物质最合适的是 A.KMnO4 B.H2O2 C.Cl2 水 D.HNO3
已知KMnO4氧化Fe2+时,生成Mn2+离子,试写出酸性KMnO4与Fe2+反应的离子反应方程式;然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3 , 可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
A.NaOH B. NH3H2O C.CuCO3 D.Cu(OH)2
(3)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10﹣38 , Cu(OH)2的溶度积Ksp=3.0×10﹣18 , 通常认为残留在溶液中的离子浓度小于1×10﹣5 molL﹣1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0molL﹣1 , 则Cu(OH)2开始沉淀时溶液的pH为 , Fe3+完全沉淀时溶液的pH为(已知lg2=0.3,lg5=0.7),通过计算确定上述方案(填“可行”或“不可行”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.
(1)我国科学家屠呦呦因发现治疗疟疾的特效药﹣﹣青蒿素,而获得2015年诺贝尔生理学或医学奖.青蒿素的结构简式如图所示,其含有的过氧基(﹣O﹣O﹣)具有强氧化性. 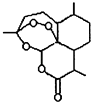
请回答下列问题:
①青蒿素的分子式为 .
②下列有关青蒿素的叙述中,正确的是(填字母).
A、青蒿素属于芳香族化合物
B、青蒿素具有强氧化性,可用于杀菌
C、青蒿素分子中的所有碳原子在同一个平面上
D、在一定条件下,青蒿素能与NaOH溶液发生反应
(2)阿司匹林(乙酰水杨酸) ![]() 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为 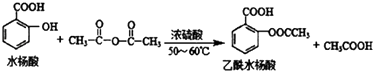
请回答下列问题:
①乙酰水杨酸中的含氧官能团的名称为
②制得的阿司匹林中常含有少量的杂质水杨酸,下列试剂可用于检验阿司匹林样品中是否混有水杨酸的是(填字母).
A、碳酸氢钠溶液 B、三氯化铁溶液 C、石蕊试液
③写出水杨酸与足量的NaHCO3溶液完全反应所得有机产物的结构简式: .
(3)丙烷的一氯代物有种,写出其一氯代物在氢氧化钠醇溶液共热条件下的有机产物的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)H2(g)+I2(g),2s时生成0.1mol H2 , 则以HI表示该时段的化学反应速率是( )
A.0.05 molLˉ1sˉ1
B.0.1 molLˉ1sˉ1
C.0.2 molLˉ1sˉ1
D.0.8 molLˉ1sˉ1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.石油的炼制过程都是化学变化过程
B.石油分馏目的是将含碳原子数较多的烃先气化经冷凝而分离出来
C.石油经过常、减压分馏、裂化等工序炼制后即能制得纯净物
D.石油分馏出来的各馏分仍是多种烃的混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com