
| A. | 金属钠着火可用水扑灭 | |
| B. | 钠可从硫酸镁溶液中置换出大量的镁 | |
| C. | 自然界可存在少量的钠单质 | |
| D. | 金属钠长期置于空气中,最终变成Na2CO3 |
分析 钠的密度大于煤油且和煤油不反应,但钠性质很活泼,易和水、氧气发生氧化还原反应而变质,钠燃烧生成过氧化钠,过氧化钠能和水、二氧化碳反应生成氧气.
解答 解:A、钠燃烧生成过氧化钠,过氧化钠和水、二氧化碳反应生成氧气,促进钠燃烧,故A错误;
B、将钠投入硫酸镁溶液中,钠先和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸镁发生反应生成难溶性的氢氧化镁白色沉淀,故B错误;
C、钠是活泼金属,在自然界只能以化合物的形式存在,故C错误;
D、金属钠露置于空气中,首先被氧化成Na2O,Na2O与水作用生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3,故D正确;
故选D.
点评 本题主要考查了钠的性质,题目难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | BaCl2溶液 | D. | Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入硫酸 | B. | 加入少量氯化铵晶体 | ||
| C. | 继续加水 | D. | 升温 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
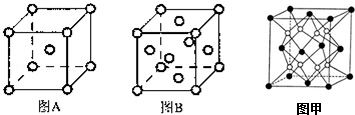
 其基态原子核外有26种不同电子运动状态;
其基态原子核外有26种不同电子运动状态;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性MnO4->Cl2>I2>Fe3+ | B. | 还原性:Fe2+>I->Cl- | ||
| C. | Fe3+能将I-氧化为I2 | D. | Fe2+只有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com