
| A����֪H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ?mol-1����H2SO4��aq��+Ba��OH��2��aq���TBaSO4��s��+2H2O��l����H=2����-57.3��kJ?mol-1 | ||||
| B����֪��H2��g��+F2��g���T2HF��g����H=-270 kJ?mol-1����1 mol������1 mol������Ӧ����2 molҺ̬������ų�������С��270 kJ | ||||
C��500�桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3 kJ�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��
| ||||
D�������ǵ�ȼ������2 800 kJ?mol-1����
|



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��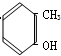 �� һCH2OH �� һCH2OH 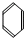 |
| B����������ͼ�ȩ |
| C��������ϩ |
| D��CH3CH2OH��CH3CH2CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+��Na+��Br-��SiO32- |
| B��H+��Fe2+��SO42-��Cl- |
| C��K+��Ca2+��Cl-��NO3- |
| D��K+��Al3+��NH3?H2O��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����С�մ�NaHCO3������θ����ࣺHCO3-+H+=CO2��+H2O |
| B������ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� |
| C�������������еμ��Ȼ�ͭ��Һ��Cu2++2OH-=Cu��OH��2�� |
| D��ͭƬ������������Һ��Cu+Ag+�TCu2++Ag |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
233 92 |
A���ˣ�U����92��Ԫ�أ�
| ||
| B��ThԪ�ص����ԭ��������231 | ||
| C��232Thת����233U�ǻ�ѧ�仯 | ||
| D��230Th��232Th�����ʲ�ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��SiO2�ǹ��������������ˮ�������ɹ��� |
| B��CO2ͨ��ˮ�����п��Եõ����� |
| C���ڸ�����SiO2��Na2CO3��Ӧ�ų�CO2�����Թ�������Ա�̼��ǿ |
| D��SiO2���������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.012 kg 12C�к���Լ6.02��1023��̼ԭ�� |
| B��1 mol H2O���2 mol���1 mol�� |
| C���������Ƶ�Ħ��������40 g |
| D��2 molˮ��Ħ��������1 molˮ��Ħ��������2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��5.6g Fe������ϡ���ᷴӦת�Ƶĵ�����Ϊ0.3NA |
| B�����³�ѹ�£�23g NO2����NA����ԭ�� |
| C����״���£�22.4Lˮ���и�NA H2O���� |
| D��1mol/L NaCl��Һ����NA��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
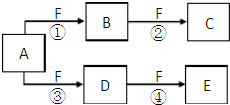 X��Y��Z�����ֶ�����Ԫ�أ�X��Z��������֮����Y����������ȣ�Z�ĵ��Ӳ�����X�ĵ��Ӳ�����2����A��B��C��D��E��F����ѧ��ѧ�еij������ʣ���������������Ԫ���е�һ�֡����ֻ�������ɣ�����A����ʹʪ���ɫʯ����ֽ���������壬D��E�������ᣬF��һ�ֵ��ʣ���Ӧ�ܾۢ������������½��У���ת����ϵ��ͼ��ʾ��
X��Y��Z�����ֶ�����Ԫ�أ�X��Z��������֮����Y����������ȣ�Z�ĵ��Ӳ�����X�ĵ��Ӳ�����2����A��B��C��D��E��F����ѧ��ѧ�еij������ʣ���������������Ԫ���е�һ�֡����ֻ�������ɣ�����A����ʹʪ���ɫʯ����ֽ���������壬D��E�������ᣬF��һ�ֵ��ʣ���Ӧ�ܾۢ������������½��У���ת����ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com