

| A. | 化合物2在一定条件下可发生加聚反应 | |
| B. | 检验制得的香草醛中是否混有化合物3,可用氯化铁溶液 | |
| C. | 理论上反应1→2中原子利用率100% | |
| D. | 化合物2→3的反应为消去反应 |
分析 A.化合物2分子中含有羧基、醇羟基,可以通过形成酯基发生缩聚反应生成高聚物;
B.香草醛与化合物3中都含有酚羟基,遇氯化铁溶液都变紫色;
C.根据化合物1、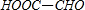 与化合物2的分子组成判断;
与化合物2的分子组成判断;
D.化合物2→3的反应为氧化反应.
解答 解:A.化合物2分子中含有羧基、醇羟基,可以通过形成酯基发生缩聚反应生成高聚物,不含碳碳双键,不能发生加聚反应,故A错误;
B.香草醛与化合物3中都含有酚羟基,遇氯化铁溶液都变紫色,故B错误;
C.由原子可知,化合物1、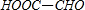 的原子全部生成化合物2,没有其它物质生成,反应1→2中原子利用率为100%,故C正确;
的原子全部生成化合物2,没有其它物质生成,反应1→2中原子利用率为100%,故C正确;
D.化合物2→3的反应为氧化反应,羟基被氧化生成羰基,故D错误.
故选C.
点评 本题以有机物合成为载体考查有机物的结构、官能团性质等,为高频考点,侧重于学生的分析能力的考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物水化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 0.3 mol/L的HCl和50 mL 0.3 mol/L的NaOH相混合 | |
| B. | 80mL 0.3 mol/L的HCl和80 mL 0.3 mol/L的NaOH溶液相混合 | |
| C. | 80mL 0.3 mol/L的H2SO4和80 mL 0.3 mol/L的NaOH溶液相混合 | |
| D. | 50mL 0.3 mol/L的H2SO4和50 mL 0.6 mol/L的NaOH溶液相混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热滴有酚酞的K2CO3(稀溶液):红色变浅 | |
| B. | 含FeCl3的溶液中滴入SCN-:溶液变为红色 | |
| C. | 将稀溴水滴入含少量的苯酚溶液中:产生白色沉淀 | |
| D. | 将硫酸铝溶液蒸干,可得固体氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;C的结构式
;C的结构式 .?
.?查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com