
| A、醋酸溶液的导电性比盐酸弱 |
| B、醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 |
| C、0.1mol L-1的CH3COOH溶液中氢离子浓度约为0.001 mol L-1 |
| D、醋酸溶液用水稀释后,氢离子浓度下降 |


科目:高中化学 来源: 题型:
A、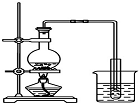 制取少量蒸馏水 |
B、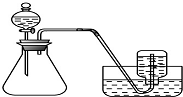 用铜和浓硝酸制取少量NO2 |
C、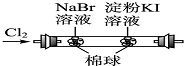 证明氧化性:Cl2>Br2>I2 |
D、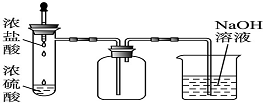 制取HCL且除去多余的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.3mol |
| B、0.025mol |
| C、0.05mol |
| D、5.55g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 |
| B、10?10:10?4 |
| C、10?4:10?10 |
| D、10?10:10?7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 | ||
| B、因含有过氧基“-O-O-”而有强氧化性 | ||
C、由下列过氧乙酸的制取原理可以看出,过氧乙酸是酯的同系物CH3COOH+H2O2
| ||
| D、过氧乙酸易分解生成乙酸和氧气,不可直接用手接触原液,使用时不可稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、着色剂-----醋酸 |
| B、疏松剂-----碳酸氢钠 |
| C、调味剂------亚硝酸钠 |
| D、防腐剂------苯甲酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3 溶液刻蚀铜制的印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| B、硅酸钠溶液和稀硫酸混合:Na2SiO3+2H+=H2SiO3↓+2Na+ |
| C、Ba(OH)2 溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向氯化铝溶液中滴加过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com