
| Kw |
| c(OH-) |
| 4×10-14 |
| 0.1 |
| 3c-2c |
| 3+2 |
| c |
| 5 |
| Kw |
| c(H+) |
| 4×10-14 |
| 10-12 |
| c |
| 5 |


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
 A《化学与生活》
A《化学与生活》查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组同学用如图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.
某课外活动小组同学用如图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
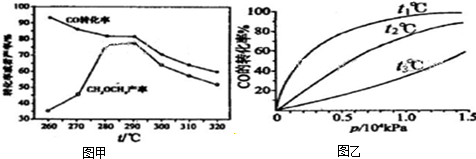
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、假设这种想法可行,则可能在制取盐酸的同时,获取电能 |
| B、负极材料是锌,正极材料是石墨,用氢氧化钠溶液作电解质溶液 |
| C、通入氢气的电极为原电池的正极 |
| D、电解质溶液中的阴离子向通氯气的电极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NH
| ||||||
| B、Ag+、Na+、[Al(OH)2]+、Cl- | ||||||
C、K+、NH
| ||||||
D、K+、Na+、NO3-、HCO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚不小心沾到皮肤上,可用酒精进行洗涤以减轻伤害 |
| B、营养物质淀粉、纤维素和蛋白质都属于高分子化合物 |
| C、提倡人们购物时不用塑料袋,是为了防止白色污染 |
| D、35%-40%甲醛溶液俗称为福尔马林,可用来浸泡海产品来起到保鲜效果 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com