
【题目】如图所示实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
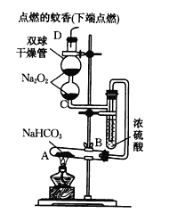
(1)在A试管内发生反应的化学方程式是_____________。
(2)B装置的作用是____________。
(3)在双球干燥管内发生反应的化学方程式为___________________,该反应中氧化剂为________,氧化产物为________,每有1molNa2O2发生反应,转移电子数目为________。
(4)双球干燥管内观察到的实验现象是_________________。
【答案】2NaHCO3![]() Na2CO3+H2O+CO2↑ 吸收气体中的水蒸气(或干燥CO2) 2Na2O2+2CO2=2Na2CO3+O2 Na2O2 O2 NA(或6.02×1023) 淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈
Na2CO3+H2O+CO2↑ 吸收气体中的水蒸气(或干燥CO2) 2Na2O2+2CO2=2Na2CO3+O2 Na2O2 O2 NA(或6.02×1023) 淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈
【解析】
根据实验装置图,可整理出实验的步骤和顺序为:A中的NaHCO3受热分解产生的CO2和H2O(g)进入试管B,H2O(g)被浓硫酸吸收,从B中出来的CO2气体与C处与D处的Na2O2反应,生成O2,从而促进蚊香的燃烧。
(1)碳酸氢钠不稳定,受热易分解,反应的化学方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(2)由于生成的CO2气体中含有水蒸气,所以浓硫酸的作用是吸收水蒸气,干燥CO2;
(3)CO2能和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2。在氧化还原中,同一元素的化合价的变化只能靠近不能交叉,因此Na2O2中的O的化合价既升高又降低,Na2O2既是氧化剂也是还原剂,因此氧化剂是Na2O2;O2是Na2O2中的O化合价升高,经氧化反应得到的氧化产物;根据化学方程式每有1molNa2O2发生反应转移电子的物质的量为1mol,其数目为NA(或6.02×1023);
(4)CO2能和过氧化钠反应生成碳酸钠和氧气,而生成的氧气可以促进蚊香燃烧,所以实验现象是淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】某温下气体反应达到化学平衡,平衡常数K=![]() ,恒容时,若温度适当降低,F的浓度增加,下列说法正确的是( )
,恒容时,若温度适当降低,F的浓度增加,下列说法正确的是( )
A.降低温度,正反应速率增大
B.增大c(A)、c(B),K增大
C.向容器中充入稀有气体X,压强增大,反应速率不变
D.该反应的化学方程式为2E(g)+F(s)![]() A(g)+2B(g)
A(g)+2B(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z 位于相同短周期,它们的最高及最低化合价如表所示,下列判断错误的是
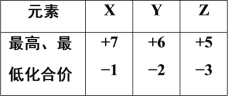
A.原子序数:X>Y>Z
B.原子半径:X>Y>Z
C.稳定性:HX>H2Y>ZH3
D.酸性由强到弱:HXO4>H2YO4>H3ZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置完成了浓硫酸和SO2性质实验(夹持装置已省略)。请回答:
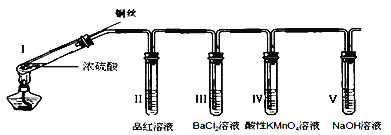
(1)下列说法正确的是__________。
A.反应后,将试管Ⅰ中的白色固体加入水中,溶液呈蓝色
B.取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO4
C.试管Ⅳ中KMnO4溶液褪色,说明SO2具有氧化性
D.试管V中的NaOH溶液可用Na2CO3溶液代替
(2)取下试管Ⅱ,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质:①Cu ②NaCl晶体 ③NaHSO4 ④CO2 ⑤稀H2SO4 ⑥C2H5OH属于电解质的是(填序号,下同)_____,属于非电解质的是_____。
(2)写出下列物质在水溶液中的电离方程式:
①NaHSO4 _______;
②Al2(SO4)3 _______;
(3)按要求写出下列方程式:
①写出硫酸铜溶液中滴加氢氧化钠溶液的反应的离子方程式:_____________。
②写出能用离子方程式CO![]() +2H+=CO2↑+H2O表示的一个化学方程式:__________。
+2H+=CO2↑+H2O表示的一个化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s)═CuSO4(s)+5H2O(l)△H=+Q2kJmol-1则Q1、Q2的关系为
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或折开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则反应P4(白磷)+3O2=P4O6的反应热ΔH为

A.-1 638 kJ/molB.+1 638 kJ/molC.-126 kJ/molD.+126 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀硝酸中,生成了6.72LNO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为
A.22.1gB.27.2gC.30gD.30.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性甲醛燃料电池为电源进行电解的实验装置如图所示,下列说法中正确的是
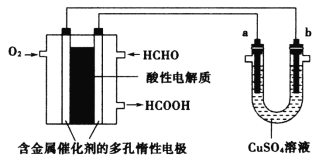
A.燃料电池工作时,负极反应为HCHO+H2O-4e-=CO2+4H+
B.当燃料电池消耗2.24L甲醛气体时,电路中理论上转移0.2mole-
C.当a、b都是铜电极时,电解的总反应方程式为:2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑
2H2SO4+2Cu+O2↑
D.电解后,消耗的甲醛和a电极上析出物质的物质的量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com