
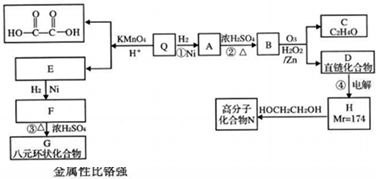
| KMnO4/H+ |
| O3 |
| H2O2/Zn |
| 120 |
| 10 |
| 16 |
| 1 |
| 48 |
| 16 |
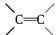 ,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有
,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有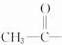 、-CH=CHCOOH,故Q的结构简式为
、-CH=CHCOOH,故Q的结构简式为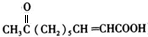 ,则E为
,则E为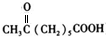 ,F为
,F为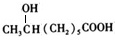 ,G为
,G为 .Q与氢气发生加成反应生成A为
.Q与氢气发生加成反应生成A为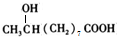 ,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为
,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为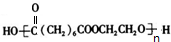 ,据此解答.
,据此解答.| 120 |
| 10 |
| 16 |
| 1 |
| 48 |
| 16 |
 ,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有
,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有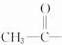 、-CH=CHCOOH,故Q的结构简式为
、-CH=CHCOOH,故Q的结构简式为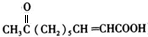 ,则E为
,则E为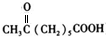 ,F为
,F为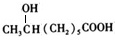 ,G为
,G为 .Q与氢气发生加成反应生成A为
.Q与氢气发生加成反应生成A为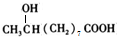 ,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为
,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为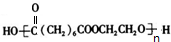 ,
,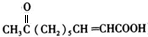 ,所含氧官能团为:羧基、羰基,故答案为:C10H16O3;羧基、羰基;
,所含氧官能团为:羧基、羰基,故答案为:C10H16O3;羧基、羰基; ,
, ;
; ,故答案为:②;
,故答案为:②; ;
;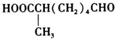 ,故答案为:15;
,故答案为:15;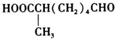 ;
; ,
, .
.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
| A、Fe+H2SO4═FeSO4+H2↑ | ||||
B、CO+CuO
| ||||
C、Cu2(OH)2CO3
| ||||
| D、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 、
、 、
、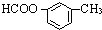 、
、查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、CH3COO-、K+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、Ca2+、Mg2+、HCO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲、乙两溶液均呈酸性 |
| B、甲、乙两溶液中c(H+)之比为1:2 |
| C、甲、乙两溶液中水的电离程度大小无法比较 |
| D、甲中水的电离程度小于乙中水的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(A-)>c(Na+) |
| B、c(HA)<c(A-) |
| C、c(Na+)>c(OH-) |
| D、c(HA)+c(A-)=0.1 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com