
| A. | 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 20g重水中含有的电子数为10NA | |
| C. | 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.3NA | |
| D. | 1L 0.1mol/L NH4Cl溶液中含NH4+数为0.1NA |
分析 A、标况下辛烷为液态;
B、求出重水的物质的量,然后根据重水中含10个电子来分析;
C、求出铁的物质的量,然后根据铁和盐酸反应后变为+2价来分析;
D、铵根离子为弱碱阳离子,在溶液中会水解.
解答 解:A、标况下辛烷为液态,故不能根据气体摩尔体积来计算其物质的量和燃烧生成的二氧化碳分子个数,故A错误;
B、20g重水的物质的量为1mol,而重水中含10个电子,故1mol重水中含10NA个电子,故B正确;
C、5.6g铁的物质的量为0.1mol,而铁和盐酸反应后变为+2价,故0.1mol铁失去0.2NA个电子,故C错误;
D、铵根离子为弱碱阳离子,在溶液中会水解,故溶液中的铵根离子的个数小于0.1NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题

| A. | M点和N点对应的溶液均呈中性 | |
| B. | T1℃时,P点对应溶液中,水电离出来的c(H+)可能为10-4mol•K-1或10-10mol•L-1 | |
| C. | T2℃时,pH=11的NaOH溶液与pH=1的稀H2SO4等体积混合,所得溶液的pH=6 | |
| D. | 向某溶液中加入酸或碱,均可以使该溶液从M点转化为N点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
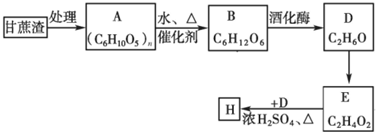
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
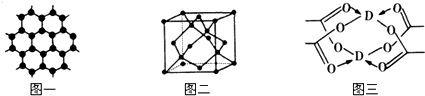
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 滤液I的主要成分是Na2SiO3、NaAlO2和NaOH | |
| B. | 滤液III的含大量的阴离子是HCO3- | |
| C. | 反应Y的离子方程式是2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| D. | 滤液II中通入过量的X的目的是使AlO2-充分沉淀而不引进杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4 | B. | KNO3 | C. | Ca(NO3)2 | D. | KIO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6g由NO2和N2O4组成的混合物中氧原子总数为0.2NA | |
| B. | 标准状况下,22.4L的SO3中含3NA个氧原子 | |
| C. | 100mL18.4mol/L的浓硫酸与足量的铜加热反应,转移的电子数为1.84NA | |
| D. | 密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数一定为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Cl?、NO3? | B. | K+、Na+、ClO?、SO42- | ||
| C. | Al3+、Cu2+、Cl?、S2- | D. | Na+、Fe2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
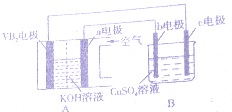 碱性硼化钒(VB2),-空气电池工作时反应为:4VB2+1lO2=4B203+2V205.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到 0.448L气体(标推状况)下列说法正确的是( )
碱性硼化钒(VB2),-空气电池工作时反应为:4VB2+1lO2=4B203+2V205.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到 0.448L气体(标推状况)下列说法正确的是( )| A. | VB2电极发生的电极反应为:2VB2+11H20-22e-═V205+2B203+22H+ | |
| B. | 若B装置内液体的体积一直为200mL,则原CuS04溶液浓度为0.05 mol/L | |
| C. | 电解过程中,b电极表面先有红色物质析出,然后有气泡产生 | |
| D. | 外电路中电子由c电极流向VB2电极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com