
- 3 |
| A、②⑥⑧ | B、④⑥⑧ |
| C、②④⑦⑧ | D、④⑧ |


科目:高中化学 来源: 题型:
 的方案中,所涉及的化学反应类型依次为( )
的方案中,所涉及的化学反应类型依次为( )| A、消去、加成、取代、取代 |
| B、消去、加成、取代、消去 |
| C、取代、加成、取代、取代 |
| D、取代、消去、取代、取代 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、是烃类化合物 |
| B、常温下呈固态 |
| C、分子中可能含不饱和碳原子 |
| D、不能在空气中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用溶解、过滤的方法分离CaCl2和NaCl的固体混合物 |
| B、用BaCl2除去NaOH溶液中混有的少量Na2SO4 |
| C、用酒精把碘水中的碘萃取出来 |
| D、用澄清石灰水检验CO中是否含有CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
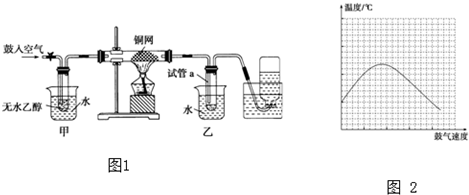
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| 序号 | 碳粉的质量/g | 氮气的物质的量/mol | 二氧化硅的质量/g | 二氧化硅的形状 | 反应温度/℃ | 达到平衡所用的时间/s | 平衡时氮化硅的质量/g |
| 1 | 7.2 | 3.0 | 12.0 | 大颗粒 | 1500 | 300 | m1 |
| 2 | 7.2 | 3.0 | 12.0 | 大颗粒 | 1550 | 200 | m2 |
| 3 | 7.2 | 3.0 | 12.0 | 小颗粒 | 1550 | 120 | m3 |
| 4 | 7.2 | 3.0 | 12.0 | 小颗粒 | 1600 | 80 | 6.3 |
| 5 | 7.2 | 3.0 | 12.0 | 粉末 | 1550 | t1 | 7.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示已知:
如图所示已知:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com