
分析 结构相似,分子组成相差n个CH2原子团的有机物互为同系物;
具有相同分子式、不同结构的有机物互为同分异构体;
同种元素的不同单质,互为同素异形体;
具有相同质子数、不同中子数的原子为同位素;
分子式相同、结构相同的物质为同一种物质;
根据以上概念进行判断.
解答 解:①O2 ②CH3OH ③CH3CH2CH2OH ④O3 ⑤CHCl3 ⑥CH3OCH2CH3 ⑦126C ⑧CH3CH(OH)CH3 ⑨136C ⑩三氯甲烷,以上组物质中,③CH3CH2CH2OH和②CH3OH、⑧CH3CH(OH)CH3和②CH3OH的结构相似,分子组成相差n个CH2原子团的有机物,它们互为同系物;
③CH3CH2CH2OH、⑥CH3OCH2CH3、⑧CH3CH(OH)CH3具有相同分子式、不同结构的有机物,二者互为同分异构体;
①O2④O3为同种元素的不同单质,互为同素异形体;
⑦126C和⑨136C为具有相同质子数、不同中子数的原子,二者为同位素;
⑩三氯甲烷⑤CHCl3 都是三氯甲烷,三氯甲烷不存在同分异构体,所以二者为同种物质,
故答案为:②③或②⑧;③⑥⑧;①④;⑦⑨;⑤⑩.
点评 本题考查较综合,涉及有机物的结构与性质、相关概念的辨析等,把握有机物中官能团与性质的关系为解答的关键,题目综合性强,但难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 分离、提纯→确定化学式→确定实验式→确定结构式 | |
| B. | 分离、提纯→确定结构式→确定实验式→确定化学式 | |
| C. | 分离、提纯→确定实验式→确定化学式→确定结构式 | |
| D. | 确定化学式→确定实验式→确定结构式→分离、提纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成氨时,其他条件不变升高温度,反应速率v(H2)和氢气的平衡转化率均增大 | |
| B. | 3C(s)+CaO(s)=CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 | |
| C. | 向氨水中不断通入CO2,随着CO2的增加,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断增大 | |
| D. | 铁表面镀铜时,铁与电源的正极相连,铜与电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 压强/Mpa C% 温度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
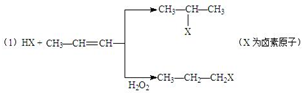
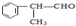 的物质,该物质是一种香料.
的物质,该物质是一种香料.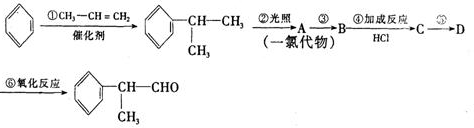
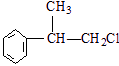 、
、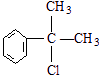 .
.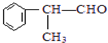 的官能团的名称醛基.
的官能团的名称醛基.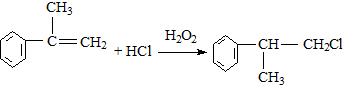 .
.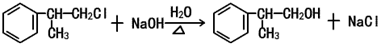 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
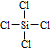 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将得到的m g固体放到氧气中充分灼烧后,固体质量变为4.8 g | |
| B. | 生成的CO2已被Ba(OH)2溶液完全吸收,Ba2+沉淀完全 | |
| C. | Ba(OH)2溶液吸收CO2后的溶液中有BaCO3和Ba(HCO3)2,且物质的量的比为2:1 | |
| D. | 原混合物中CuO与Fe2O3的质量比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com