
氧化铜矿石含有CuO和Cu2(OH) 2CO3,还含有Fe2O3、FeO和SiO2等。铜、铁是畜禽所必需的微量元素。某饲料厂联合生产硫酸铜和硫酸亚铁工艺流程如下:
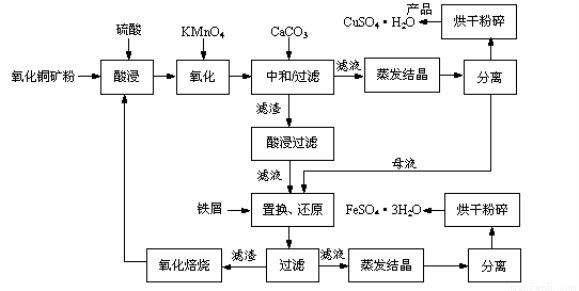
(1)氧化铜矿石粉碎的目的是 。
(2)写出“酸浸”中Cu2(OH) 2CO3发生反应的离子方程式 。
(3)“中和/过滤”中加入CaCO3的目的是 。
(4)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 。
(5)加入铁屑的作用是 、 。
(6)下表和下图为“烘干粉碎”的试验结果。

硫酸亚铁干燥曲线图
序号 | t/h | t/℃ | m/g | x |
1 | 3 | 80 | 5 | 4 |
2 | 3 | 160 | 10 | 1 |
3 | 4 | 160 | 10 | 0.8 |
4 | 4 | 160 | 5 | 0 |
5 | 5 | 80 | 5 | 3 |
6 | 5 | 160 | 15 | 1 |
表2.硫酸铜晶体(CuSO4·5H2O)干燥试验表
表2中,m为CuSO4·5H2O晶体的质量,x为干燥后所得晶体中结晶水的个数。据此可确定由CuSO4·5H2O和FeSO4·7H2O脱水得流程中所示产品的适宜工艺条件分别为 , (分别指出两条件的温度和时间)。
(1)增大接触面积,加快化学反应速率;(2)Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑;(3)适当降低溶液的酸性,使Fe3+水解成沉淀而除出;(4)烧杯、玻璃棒、漏斗;(5)使母液中Fe3+ 转化为Fe2+、除去Cu2+,提高硫酸亚铁晶体的纯度;(6)160℃、3h,125(±5)℃、4.0h。
【解析】
 试题分析:(1)氧化铜矿石是固体物质,粉碎是为了增大接触面积,加快化学反应速率;(2)Cu2(OH) 2CO3与硫酸发生反应符合复分解反应的规律。其离子方程式为Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑。(3)“中和/过滤”中加入CaCO3的目的是为了适当降低溶液的酸性,使Fe3+水解成沉淀而除出;(4)在实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗;(5)加入铁屑时发生反应:Fe+ 2Fe3+=3Fe2+;:Fe+ Cu2+= Fe2++Cu.因此加入Fe屑的作用是为了使母液中Fe3+ 转化为Fe2+、除去Cu2+,从而可以提高硫酸亚铁晶体的纯度;(6)由CuSO4·5H2O制取CuSO4·H2O,根据表二提供的数据可知反应条件是160℃、3h;而由FeSO4·7H2O脱水制取FeSO4·3H2O,根据图六硫酸亚铁干燥曲线图可知反应条件为125(±5)℃、4.0h。
试题分析:(1)氧化铜矿石是固体物质,粉碎是为了增大接触面积,加快化学反应速率;(2)Cu2(OH) 2CO3与硫酸发生反应符合复分解反应的规律。其离子方程式为Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑。(3)“中和/过滤”中加入CaCO3的目的是为了适当降低溶液的酸性,使Fe3+水解成沉淀而除出;(4)在实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗;(5)加入铁屑时发生反应:Fe+ 2Fe3+=3Fe2+;:Fe+ Cu2+= Fe2++Cu.因此加入Fe屑的作用是为了使母液中Fe3+ 转化为Fe2+、除去Cu2+,从而可以提高硫酸亚铁晶体的纯度;(6)由CuSO4·5H2O制取CuSO4·H2O,根据表二提供的数据可知反应条件是160℃、3h;而由FeSO4·7H2O脱水制取FeSO4·3H2O,根据图六硫酸亚铁干燥曲线图可知反应条件为125(±5)℃、4.0h。
考点:考查反应条件的选择、化学方程式、离子方程式的书写的知识。


科目:高中化学 来源:2013-2014学年河南省商丘市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物。
(1)为快速得到乙醇气体,可采取的方法是 ;
若实验时小试管中的溶液已经开始发生倒吸,你采取的措施是 (填写编号);
a.取下小试管 b.移去酒精灯 c.将导管从乳胶管中取下 d.以上都可以
(2)盛Cu(OH)2悬浊液的试管中出现的现象为 。
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热。为了检验M的组成,进行下列实验。

①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
② 经检验溶液中有Fe2+和Fe3+,检验该溶液中的Fe2+的方法是 ;
关于M中铁元素价态的判断正确的是 (填写编号)。
a.一定有+3价和+2价铁,无0价铁
b.一定有+3价、+2价和0价铁
c.一定有+3价和0价铁,无+2价铁
d.一定有+3和+2价铁,可能有0价铁
(4)若M的成份可表达为FeXOY,用CO还原法定量测定其化学组成。称取a g M样品进行定量测定,实验装置和步骤如下:
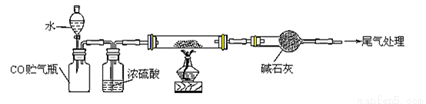
①组装仪器;②点燃酒精灯;③加入试剂; ④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……。正确的操作顺序是 (填写编号)
a.①⑤④③②⑥⑦⑧ b.①③⑤④②⑦⑥⑧ c.①⑤③④②⑥⑦⑧ d.①③⑤②④⑥⑦⑧
(5)若实验中每步反应都进行完全,反应后M样品质量减小b g,则FexOy中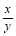 = 。
= 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省南昌市高三3月第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列实验的操作、现象和解释或结论都正确的是
| 操作 | 现象 | 解释或结论 |
A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 |
C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | Al3++3H2O |
D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+=Cu+2Na+ |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省高三百校联合调研测试(一)化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是

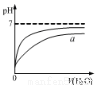
图甲 图乙 图丙 图丁
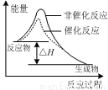
A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B.图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸
C.图丙表示该反应为放热反应,且催化剂能改变反应的焓变
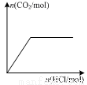
D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省高三百校联合调研测试(一)化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.SO2具有氧化性,可用于漂白纸浆
B.炭具有还原性,一定条件下能将二氧化硅还原为硅
C.BaCO3、BaSO4都难溶于水,均可用做钡餐
D.Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省高三年级模拟考试化学试卷(解析版) 题型:选择题
下列有关物质浓度关系的描述中,正确的是
A.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42—)>c(OH—)=c(H+)
B.25℃时,NaB溶液的pH=8,c(Na+) + c(B-)=9.9×10-7mol·L-1
C.0.1 mol·L-1的NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D.同温下,pH相同时,溶液物质的量浓度:c(CH3COONa)<c(NaHCO3)<c(C6H5ONa)<c(Na2CO3)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省高三年级模拟考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是
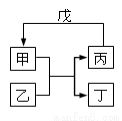
| 甲 | 乙 | 丙 | 戊 |
① | NH3 | O2 | NO | H2O |
② | Fe | H2O | H2 | Fe2O3 |
③ | Al2O3 | NaOH溶液 | Na AlO2溶液 | 过量CO2 |
④ | Na2O2 | CO2 | O2 | Na |
A.①③ B.②③ C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省南京市、盐城市高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.反应SiO2(s)+ 3C(s) = SiC(s) + 2CO(g)室温下不能自发进行,则该反应的△H<0
B.铅蓄电池放电过程中,正极质量增加,负极质量减小
C.25℃下,在NH3·H2O稀溶液中,加水,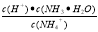 的值不变
的值不变
D.在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-水解程度增大,pH增大
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省肇庆市高三级第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式,不正确的是
A.工业上可用电解法制备Mg:MgCl2(熔融)  Mg + Cl2↑
Mg + Cl2↑
B.向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2=2HClO+CaCO3↓
C.用CaSO4治理盐碱地:CaSO4(s) + Na2CO3(aq) CaCO3(s) + Na2SO4(aq)
CaCO3(s) + Na2SO4(aq)
D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72- + Fe2+ + 14H+ == 2Cr3+ + Fe3+ + 7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com