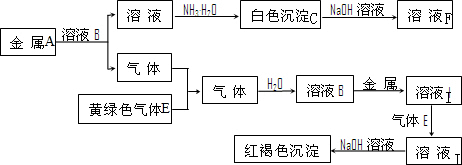
按要求回答下列问题
(1)用离子方程式解释纯碱溶液去除油污的原因:
CO32-+H2O?HCO3-+OH-;HCO3-+H2O?H2CO3+OH-
CO32-+H2O?HCO3-+OH-;HCO3-+H2O?H2CO3+OH-
(2)写出泡沫灭火器中反应的离子方程式[内液:Al
2(SO
4)
3,外液:NaHCO
3]:
3HCO3-+Al3+=Al(OH)3↓+3CO2↑
3HCO3-+Al3+=Al(OH)3↓+3CO2↑
(3)SOCl
2是一种液态化合物,沸点为77℃.向盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl
2,可观察到剧烈反应,液面上有白雾生成,并有无色有刺激性气味气体逸出,该气体中含有使品红溶液褪色的SO
2,根据实验现象,写出SOCl
2与水反应的化学方程式:
SOCl2+H2O=2HCl↑+SO2↑
SOCl2+H2O=2HCl↑+SO2↑
删去此空
删去此空
蒸干AlCl
3溶液不能得到无水AlCl
3,使SOCl
2与AlCl
3?6H
20混合并加热,可得到无水AlCl
3,解释原因:
反应产生的氯化氢气体会抑制铝离子的水解
反应产生的氯化氢气体会抑制铝离子的水解
(4)已知:铅蓄电池总的化学方程式为:Pb+PbO
2+2H
2SO
4 2PbSO
4+2H
2O
①铅蓄电池在放电时负极反应为
Pb+SO42--2e-=PbSO4
Pb+SO42--2e-=PbSO4
,
②铅蓄电池在充电时阳极反应为
PbSO4+2H2O-2e-=4H++SO42-+PbO2
PbSO4+2H2O-2e-=4H++SO42-+PbO2
;
③如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H
2SO
42
2
mol.
(5)常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,求出混合液中下列算式的精确计算结果(填具体数字):
c(OH
-)-c(HA)=
10-8
10-8
mol/L.



 A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化关系如图所示(部分产物已略去).
A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化关系如图所示(部分产物已略去). H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH- H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH-