
【题目】关于元素周期表的叙述中,不正确的是
A.俄国化学家门捷列夫编制了第一个元素周期表
B.元素周期律是由原子核外电子排布的周期性变化引起的
C.在元素周期表的过渡元素区域中寻找制催化剂的元素
D.元素周期表中最右上角元素的非金属性最强
 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组同学进行乙醛的银镜反应,实验操作步骤如下:
A.在试管里先注入少量NaOH溶液,振荡,然后加热煮沸。把NaOH溶液倒去后,再用蒸馏水洗净试管备用。
B.在洗净的试管里配制银氨溶液。
C.沿试管壁加入乙醛稀溶液。
D.加热。请回答下列问题:
(1)步骤A中加NaOH溶液振荡,加热煮沸的目的是_____________。
(2)步骤D应选择的加热方法是_____________(填下列装置编号)
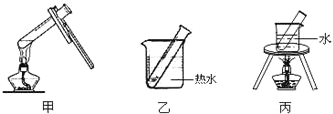
(3)乙醛发生银镜反应的化学方程式为____________________________________。
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如下表):

①实验1和实验3,探究的是_________________________。
②当银氨溶液的量为1 mL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为_____________min。(填范围)
③你认为探究乙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成银镜的_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有100 mL 3 mol·L-1 NaOH溶液和100 mL 1 mol·L-1的AlCl3溶液,①将NaOH溶液分多次加到AlCl3溶液中。②将AlCl3溶液分多次加到NaOH溶液中,比较两种操作是
A. 现象相同,沉淀质量不等 B. 现象相同,沉淀质量也相等
C. 现象不同,沉淀质量不等 D. 现象不同,沉淀质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R为原子序数依次增大的短周期元素。化合物甲由X、Z、W三种元素组成,常温下0.1mol/L甲溶液的pH=13。工业上常通过电解饱和WR溶液制得甲。Y的单质与由Y、Z组成的化合物之间的转化关系如图。下列叙述正确的是

A. 简单离子的半径:W>Z>R
B. XR与XRZ均为强酸
C. 化合物W2Z3中既含离子键又含极性键
D. 图中转化过程发生的反应均为化合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:

(1)从能量的角度看,旧键断裂,新键形成必然有能量变化.已知拆开1molH﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由氢气和碘反应生成2mol HI需要_______(填“放出”或“吸收”)_______kJ的热量.
(2)在生产和生活中经常遇到化学能与电能的相互转化.
在如图甲、乙两装置中,甲中负极电极反应式为__________________,溶液中的阴离子向______极移动(填“Zn”或“Pt”);乙中铜电极作_______极,发生_______反应(填“氧化”或“还原”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式不正确的是( )
A. 硫酸型酸雨的形成会涉及反应:2H2SO3+O2===4H++2SO![]()
B. 热的纯碱溶液可以清洗油污的原因:CO![]() +2H2O
+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C. 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-===SiO![]() +H2O
+H2O
D. 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+===Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白炭黑(SiO2·nH2O)广泛用于硅橡胶、塑料、油漆涂料等,制备白炭黑的方法主要有两种。
(l)向硅酸钠溶液中通人热的HCl气体来制取白炭黑。
① 氯化氢的电子式为________。常温下Na2SiO3溶液的pH_______(填“>”“<”或“=” ) 7。
② 用化学方程式表示该制备原理:____________。
(2)以红土镍矿(含SiO2、MgO、Fe2O3、NiO等)为原料制取白炭黑,其工艺流程如图所示。

① 步骤1熔融反应器适宜的材质是_________(填“陶瓷”“玻璃”或“不锈钢”)。
② 步骤Ⅱ在稍低于100℃ 时进行水浸的目的是___________
③ 步骤Ⅳ通入过量二氧化碳并控制pH=8-9,碳酸化时发生反应的离子方程式为_____________
④ 向步骤V过滤得到的滤液中加人石灰乳,发生苛性化反应,会重新生成Na0H,该反应的化学方程式为____________。
⑤ 步骤Ⅵ酸洗后再进行水洗,某同学为加快洗涤速率,将水洗换为用无水酒精洗涤,该同学的操作___________(填“正确”或“不正确”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
C | 向含有酚酞的Na2CO3溶液中加入少量的BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
D | 向亚硫酸钠试样中滴入盐酸酸化的Ba(ClO)2溶液 | 产生白色沉淀 | 试样已氧化变质 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com