
| A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量 |
| B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ |
| C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量 |
| D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量 |


 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源:不详 题型:单选题
| A.①>②>③>④>⑤ | B.②>①>③>④>⑤ |
| C.②>③>④>①>⑤ | D.⑤>④>③>②>① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.2A ( l ) + B ( l ) =" 2C" ( g ) ΔH1 | B.2A ( g ) + B ( g ) =" 2C" ( g ) ΔH2 |
| C.2A ( g ) + B ( g ) =" 2C" ( l ) ΔH3 | D.2A ( l ) + B ( l ) =" 2C" ( l ) ΔH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.由C(金刚石)→C(石墨)ΔH= -1.9KJ/mol 可知,金刚石比石墨稳定 |
| C.由2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1可知,H2的燃烧热为-571.6 kJ·mol-1 |
| D.稀溶液中:H+(aq)+OH—(aq)=H2O(l) ΔH= —53.7KJ/mol ,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( ) | A.一定小于92.0 kJ | B.一定大于92.0 kJ |
| C.一定等于92.0 kJ | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.已知C(石墨,s) C(金刚石,s);△H>0,则金刚石比石墨稳定 C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| B.已知C(s)+O2(g)=CO2(g);△H1和C(s)+1/2O2(g)=CO(g);△H2,则△H1>△H2 |
| C.101kPa时,2H2(g)+O2(g)=2H2O(l);△H=-5716kJ/mol,则氢气的燃烧热为285.8kJ/mol |
| D.含20.0gNaOH的稀溶液与稀盐酸完全中和时放出28.7kJ的热量,则该反应的热化学方程式为: NaOH(aq)+HCl(aq)="NaCl(aq)+" H2O(1);△H="+57.4" kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
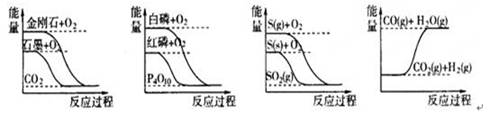
| A.白磷比红磷稳定 |
| B.石墨转变为金刚石是吸热反应 |
| C.S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2则△H1>△H2 |
| D.CO(g)+H2O(g)=CO2(g)+ H2 (g);△H1>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.图1表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图2表示0.1000mol?L—1 NaOH溶液滴定20.00mL 0.1000mol?L—1 CH3COOH溶液的滴定曲线 |
| C.图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D.图4表示某可逆反应生成物的量随反应时间的变化,t时V正<V逆 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com