
����Ŀ��ij�л���A��C4H6O5���㷺����������ˮ���ڣ�����ƻ�������ѡ����ϡ�ɽ���Ϊ�࣬��һ�ֳ��õ�ʳƷ���Ӽ����û���������������ʣ�����25��ʱ��A�ĵ���ƽ�ⳣ��K1=3.9��10-4��K2=5.5��10-6��A+RCOOH����ROH��![]() ����ζ�IJ����1molA
����ζ�IJ����1molA![]() ��������1.5mol����ܺ˴Ź������ױ���A��������5�ֲ�ͬ��ѧ��������ԭ�ӣ���A��صķ�Ӧ��ͼ���£�
��������1.5mol����ܺ˴Ź������ױ���A��������5�ֲ�ͬ��ѧ��������ԭ�ӣ���A��صķ�Ӧ��ͼ���£�
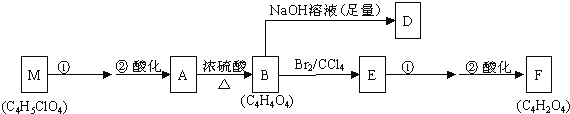
��1�����ݻ�����A�����ʣ���A�Ľṹ���������ж���______��
��a���϶���̼̼˫����b���������Ȼ���c���϶����ǻ���d����-COOR������
��2��д��A��D��F��M�Ľṹ��ʽ��A��____________��D��______��F��______��M��______��
��3��д��A��B��B��E�ķ�Ӧ���ͣ�A��B____________��B��E_________________��
��4��д��M��A�ĵڢٲ���Ӧ�ķ�Ӧ������________________��д��E��F�ĵڢٲ���Ӧ�ķ�Ӧ����ʽ��______________________��
��5���ڴ��������£�B���Ҷ����ɷ������۷�Ӧ�����ɵĸ߷��ӻ������������첣���֣�д���÷�Ӧ�Ļ�ѧ����ʽ��____________________��
��6��д��һ����A������ͬ�����ŵ�A��ͬ���칹��Ľṹ��ʽ______________________��
���𰸡� �������1����b����c�� �������2��HOOCCH��OH��CH2COOH �������3��NaOOCCH=CHCOONa �������4��HOOCC��CCOOH �������5��HOOCCH��Cl��CH2COOH �������6����ȥ��Ӧ �������7���ӳɷ�Ӧ �������8����������ˮ��Һ������ �������9��HOOCCH��Br��CH��Br��COOH+4NaOH![]() NaOOCC��CCOONa+2NaBr+4H2O �������10��n
NaOOCC��CCOONa+2NaBr+4H2O �������10��n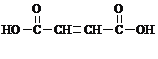 +nHOCH2CH2OH
+nHOCH2CH2OH![]()
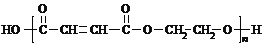 +��2n-1��H2O �������11��
+��2n-1��H2O �������11��
�����������⿼���л���ĺϳɺ��ƶϡ���1��������Ϣ������������ƽ�ⳣ����˵���Ƕ�Ԫ�ᣬ���������Ȼ���������Ϣ�ڣ�����RCOOH��ROH����������Ӧ��˵�������Ȼ����ǻ������ѡ��b��c��ȷ����2��������Ϣ�ۣ�1mol���л������������Ʒ�Ӧ����1.5mol��������1molA�к���2mol�Ȼ���1mol�ǻ���A��������5�ֲ�ͬ��ѧ��������ԭ�ӣ�����A�ķ���ʽ���Ƴ�A�Ľṹ��ʽΪHOOCCH(OH)CH2COOH���Ա�A��B�ķ���ʽ��B��A����һ��H2O��A��B������ȥ��Ӧ��B�Ľṹ��ʽΪHOOCCH=CHCOOH��B�к����Ȼ�����NaOH�����кͷ�Ӧ����D�Ľṹ��ʽΪNaOOCCH=CHCOONa��B�к���̼̼˫������Br2�����ӳɷ�Ӧ����E�Ľṹ��ʽΪNaOOCCHBr��CHBrCOONa���Ա�E��F�ķ���ʽ����Ӧ�ٷ�����ȥ��Ӧ����F�Ľṹ��ʽΪ��HOOCC��CCOOH������A�Ľṹ��ʽ���Ƴ�M��Cl��λ��A���ǻ���λ�ã�M�Ľṹ��ʽΪHOOCCHClCH2COOH����3�����ݣ�2���ķ���A��B��Ӧ����Ϊ��ȥ��Ӧ��B��E�����ӳɷ�Ӧ����4���Ա�M��A��һ������ˮ�ⷴӦ���ǻ�ȡ��Cl��λ�ã���������NaOHˮ��Һ�������ȣ�E��F��һ��������ȥ��Ӧ���䷴Ӧ����ʽΪ��HOOCCH��Br��CH��Br��COOH+4NaOH![]() NaOOCC��CCOONa+2NaBr+4H2O ����5��1molB�к���2mol�Ȼ����������۷�Ӧ���䷴Ӧ����ʽΪ n
NaOOCC��CCOONa+2NaBr+4H2O ����5��1molB�к���2mol�Ȼ����������۷�Ӧ���䷴Ӧ����ʽΪ n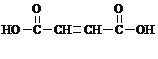 +nHOCH2CH2OH
+nHOCH2CH2OH![]()
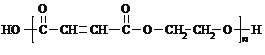 +��2n-1��H2O����6����A������ͬ�����ţ�����2���Ȼ���1���ǻ��������Ȼ���ͬһ��̼ԭ���ϣ��ǻ��ƶ�λ�ã���ͬ��ͬ�칹����
+��2n-1��H2O����6����A������ͬ�����ţ�����2���Ȼ���1���ǻ��������Ȼ���ͬһ��̼ԭ���ϣ��ǻ��ƶ�λ�ã���ͬ��ͬ�칹���� ��
��


 Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д� Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ũ�����˵����ȷ����
A. �ѻӷ� B. ����ˮ��
C. ��������ʹ��Ƭ�ۻ� D. ��������ɫ�Լ�ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����һ��ȼ�ϵ�أ�����ȼ��ΪH2�Ϳ����������Ϊ���ڵ�K2CO3���ش���������
��CO![]() ����____________����
����____________����
��������ӦʽΪ____________________��
�۵����CO![]() �����ʵ�������________________���������١����䣩��
�����ʵ�������________________���������١����䣩��
��2��������ĵ�ض������ʽ��е�⣬����a��b��c��d��e��f�缫��Ϊ���Ե缫��ͨ���a���������������Զ���b����2���Ӻ���ҳص�pHΪ12����
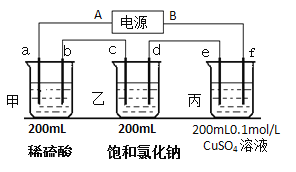
�ٵ�ԴA����______________����
��c���ϵĵ缫��Ӧʽ��___________________��
�ۼס������ع����ռ���________mol���塣
�ܱ�װ����ij������������________�ˣ���Һ��pHΪ________________�������£���������Һ����仯��
�ݵ��n���Ӻ�����ͭ���������꣬�ٽ�e��f�缫���ӵ�Դ����ͬ���ĵ����ٵ��n���ӣ������Һ�е�����ͭ�����ʵ���Ũ��Ϊ______________mol/L������������Һ����仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������в����ڸ߷��ӻ��������
A. ������ B. �Ҵ� C. ���� D. ����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A(g)��5B(g) ��4C(g)��6��(g)����5 L���ܱ������н��У�����Ӻ�C�����ʵ���������0��30 mol������������ȷ����
A�������к�D���ʵ�������Ϊ0��45 mol
B��A��ƽ����Ӧ������0��010 mol��L��1��s��1
C��������A��B��C��D�����ʵ���֮��һ����4��5��4��6
D��������A�����ʵ���һ��������0��30 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧʽ��ֻ�ܱ�ʾһ�����ʵ���(����)
A. C3H7OH B. CH2O C. C2H6O D. C3H6O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50 m L 0.1mol/L Na2S ��Һ����μ���50 mL 0.1mol/L KHSO4��Һ��������Һ������Ũ�ȹ�ϵ��ȷ����
A. c(SO42-)= c(HS-)= c(K+)>c(OH-)= c(H+)
B. c(Na+)> c(K+)> c(S2-)> c(H+)> c(OH-)
C. c(Na+)= c(S2-)+ c(HS-)+ c(H2S)+ c(SO42-)
D. c(K+)+ c(Na+)+ c(H+)= c(SO42-)+ c(S2-)+ c(HS-)+ c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A��B�ķ���ʽ��ΪC11H12O5�����ܷ������±仯��

��֪����A��B��C��D������NaHCO3��Ӧ��
��ֻ��A��D����FeCl3��Һ������ɫ��Ӧ��A�����ϵ�һ�����ֻ�����֣�
��F��ʹ��ˮ��ɫ�Ҳ����м���
��H�ܷ���������Ӧ��
��������ش��������⡣
(1)��Ӧ���ķ�Ӧ����________����Ӧ����������________��
(2)д��F�Ľṹ��ʽ________��D�к��������ŵ�������________��
(3)E��C�����۲�����д����Ӧ���Ļ�ѧ����ʽ______________________��
(4)���й���A��I��˵������ȷ����________(ѡ����)��
a��I�Ľṹ��ʽΪ
b��D��һ��������Ҳ���Է�Ӧ�γɸ߾���
c��G����8Ԫ��״�ṹ
d����������A��B�ֱ�������NaOH��Һ��Ӧ�����ĵ�����NaOH
(5)д��B������NaOH��Һ���ȵĻ�ѧ����ʽ��_____________________��
(6) D��ͬ���칹���кܶ�����д��ͬʱ��������Ҫ�������һ��ͬ���칹��Ľṹ��ʽ��_________________________��
������FeCl3��Һ������ɫ��Ӧ
���ܷ���������Ӧ������ˮ��
�������ϵ�һ±����ֻ��2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com