
【题目】一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)CH3OCH3(g)+H2O(g)
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是( )
A.该反应的正方应为吸热反应
B.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
【答案】B
【解析】解:A.容器Ⅰ中平衡时c(CH3OCH3)=c(H2O)= ![]() =0.080mol/L,c(CH3OH)=
=0.080mol/L,c(CH3OH)= ![]() =0.04mol/L,容器Ⅰ中化学平衡常数K1=
=0.04mol/L,容器Ⅰ中化学平衡常数K1= ![]() =4,容器Ⅲ中平衡时c(CH3OCH3)=c(H2O)=
=4,容器Ⅲ中平衡时c(CH3OCH3)=c(H2O)= ![]() =0.090mol/L,c(CH3OH)=
=0.090mol/L,c(CH3OH)= ![]() =0.02mol/L,化学平衡常数K2=
=0.02mol/L,化学平衡常数K2= ![]() =20.25>4,所以降低温度,化学平衡常数增大,反应向正反应方向移动,则正反应是放热反应,故A错误;
=20.25>4,所以降低温度,化学平衡常数增大,反应向正反应方向移动,则正反应是放热反应,故A错误;
B.c(CH3OH)=0.1mol/L、c(CH3OCH3 )=0.15mol/L、c(H2O)=0.10mol/L,浓度商= ![]() =1.5<4,平衡向正反应方向移动,故B正确;
=1.5<4,平衡向正反应方向移动,故B正确;
C.容器I中的温度比容器III的温度高,温度越高反应速率越快,达到平衡所需时间越短,故C错误;
D.恒容条件下,容器Ⅱ相当于在容器Ⅰ的基础上加压,但由于该反应是反应前后气体体积不变的反应,因此平衡不移动,所以容器Ⅰ中的CH3OH体积分数和容器Ⅱ中的相等,故D错误;
故选B.
A.根据温度与化学平衡常数的关系确定反应热;
B.根据化学平衡常数与浓度商的相对大小判断反应方向,如果浓度商小于平衡常数,则平衡向正反应方向进行;
C.温度越高,反应速率越大,反应时间越短;
D.该反应是反应前后气体体积不变的反应,温度相同,化学平衡常数相同,反应物的转化率相同.


科目:高中化学 来源: 题型:
【题目】NH2OH(羟胺)是一种无色针状结晶,羟胺及其盐类常用作有机合成的还原剂。回答下列问题:
(1) NH2OH的电子式为________________。
(2)拉西法制备羟胺的总反应为2NO2-+4SO2+6H2O+6NH3=4SO42-+6NH4++2NH2OH。该反应中NH3__________(填“作氧化剂”“作还原剂”或“既不作氧化剂又不作还原剂”)。
(3)室温时,NH2OH会发生分解反应,分解产生的无色气体遇浓盐酸产生白烟,与空气接触变为红棕色;且其分解产物会使无水CuSO4变蓝色,则NH2OH分解反应的化学方程式为______________________。
(4)催化还原NO是制备盐酸羟胺的一种方法,其反应原理如下:2NO+3H2+2HCl![]() 2NH2OH·HCl,某校合作学习小组的同学设计了如图所示装置制备盐酸羟胺:
2NH2OH·HCl,某校合作学习小组的同学设计了如图所示装置制备盐酸羟胺:

①该实验适宜的加热方式为______________。
②装置中导管X的作用是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H3PO2(次磷酸)是一种一元弱酸,H3PO2易溶于水且具有较强的还原性。
(1)H3PO2的结构式为____________________。
(2)H3PO2在水溶液中的电离方程式为_____________________。
(3)不断将新制的PH3通入搅拌的碘悬浮液中,直至碘的颜色消失,可得到次磷酸和氢碘酸,则该反应中氧化产物与还原产物的物质的量之比为__________________。
(4)酸性条件下,H3PO2可将Cr2O72-还原为Cr3-,其本身被氧化为磷酸,该反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)=2CO2(g)△H=﹣566kJmol﹣1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=﹣452kJmol﹣1
根据以上热化学方程式判断,下列说法正确的是( )
A.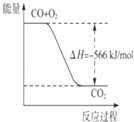
图可表示由CO生成CO2的反应过程和能量关系
B.CO的燃烧热为566 kJ/mol
C.Na2O2(s)+CO2(s)=Na2CO3(s)+ ![]() ?O2(g)△H=﹣226 kJ/mol
?O2(g)△H=﹣226 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.石油裂解气能使溴水褪色
B.可利用生活垃圾中的生物质能焚烧发电
C.水煤气既可用来合成液态烃,也可以用来合成甲醇等含氧有机物
D.煤中含有苯和二甲苯等物质,可通过煤的干馏获得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是
A. Ag+、K+、NO3-、C1- B. Mg2+、Na+、Cl-、SO42-
C. NH4+、Cu2+、OH-、Cl- D. H+、Na+、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量CO2与足量C在体积可变的恒压密闭容器中发生反应:C(s)+CO2(g) ![]() 2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:

下列说法不正确的是
A. 550℃时,v逆小于925℃时v逆
B. 650℃时,反应达平衡后,CO2的转化率为25%
C. 由图中数据分析可得,该反应为放热反应
D. T℃时,若向平衡体系内充入惰性气体,化学平衡将向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com