有A、B、C、D、E、F、G七种元素核电荷数依次增加,A是非金属元素外围电子排布式为ns
n,B的价电子层电子排布ns
nnp
n,C的基态原子中2p轨道有三个未成对的单电子,D是周期表中电负性数值最大的元素,E原子核外电子数是D与C核外电子数之和,F是主族元素且与G同周期,G能形成红色(或砖红色)的G
2O和黑色的GO两种氧化物,D与F可形成离子化合物,其晶胞结构如图2所示.请回答下列问题.

(1)E的气态氧化物EO
3分子结构模型是
.
(2)CA
3极易溶于水,其原因主要是
,试判断CA
3溶于水后,形成CA
3?H
2O的最合理结构为
(填字母).
(3)从如图2中可以看出,D跟F形成的离子化合物的电子式为
;该离子化合物晶体的密度为ag?cm
-3,则晶胞的体积是
(只要求列出算式),每个D原子周围最近的F原子有
个.
(4)某科研小组为了处理污水,设计了如图3所示的装置,Ⅱ装置为BA
4燃料电池,两电极分别通入BA
4和混合气体(空气和气体甲),电解质为熔融碳酸盐.Ⅰ是污水处理的装置,其方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)
3?Fe(OH)
3具有吸附性,可吸附污物而沉积下来,有净化水的作用,向污水中加入适量的H
2SO
4的目的是
.
②为了使燃料电池乙长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为
Ⅱ装置中负极上发生的反应
.
③Ⅰ装置中碳电极是电解池的
极,Fe电极上发生的反应为
.
④Ⅱ装置中有0.8mol BA
4参加反应时,C电极理论上生成气体的体积在标准状况下为
.


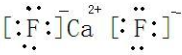 ;晶胞摩尔质量为4×(40+19×2)=312g/mol,则晶胞摩尔体积为
;晶胞摩尔质量为4×(40+19×2)=312g/mol,则晶胞摩尔体积为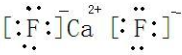 ;
;

 A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
 如图是某中学实验室的一瓶硫酸试剂标签上的部分内容.
如图是某中学实验室的一瓶硫酸试剂标签上的部分内容.
