
下列各种叙述中正确的是
A.在CH2=CH2分子中,存在4个σ键和一个π键
B.在共价化合物中,一定存在极性键,可能存在非极性键,一定不存在离子键
C.N、O、F电负性大小:F>O>N;第一电离能大小:F>O>N
D.酸性强弱:H2SO4>H2SO3>H2SeO3;岩浆晶出的先后顺序:SiO2、MgSiO3、CaSiO3
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源:2017届江苏省淮安市高三12月考试化学试卷(解析版) 题型:实验题
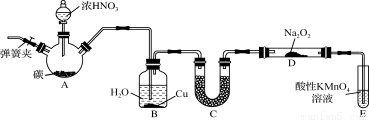
亚硝酸钠(NaNO2)是一 种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。
种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。
【背景素材】
①2NO+Na2O2===2NaNO2;
②NO能被酸性KMnO4氧化成NO ,MnO
,MnO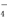 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2;S2O32-能把I2还原为I-。
【制备NaNO2】
(1) 装置A三颈烧瓶中发生反应的化学方程式为 。
(2) B装置的目的是① ,② 。
(3) 为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是 (填序号)。
A. P2O5 B. 碱石灰 C. 无水CaCl2 D. 生石灰
(4) E装置发生反应的离子方程 式是 。
式是 。
【测定NaNO2纯度】
(5) 本小题可供选择的试剂有:
A.稀硫酸
B.c1mol·L-1KI溶液
C.淀粉溶液
D.c2mol·L-1Na2S2O3溶液
E.c3mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,可选择的试剂是 (填序号)。
②利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解 (请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上12月月考化学卷(解析版) 题型:选择题
下列有关说法正确的是
A.1 mol FeBr2与足量氯气反应时,理论上转移的电子数约为3×6.02×1023
B.常温下,pH均为3的三种溶液:①HCl溶液 ②H2SO4溶液 ③CH3COOH溶液,各自溶质的物质的量浓度大小顺序为①=②<③
C.电解熔融NaCl或AlCl3制取Na或Al
D.一定条件下反应Cr2O72-(aq)+H2O(l) 2CrO42-(aq)+2H+(aq)达到平衡后,滴加少量浓硫酸(温度及体积变化忽略不计),重新达平衡前,2v正(Cr2O72-)<v逆(CrO42-)
2CrO42-(aq)+2H+(aq)达到平衡后,滴加少量浓硫酸(温度及体积变化忽略不计),重新达平衡前,2v正(Cr2O72-)<v逆(CrO42-)
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上模拟四化学试卷(解析版) 题型:选择题
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32?、SO42?、NO3?中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是

A.溶液中一定不含CO32?,可能含有SO42?和NO3?
B.溶液中n(NH4+)=0.2mol
C.溶液中的阳离子只有H+、Mg2+、Al3+
D.n(H+)∶n(Al3+)∶n(Mg2+ ) = 1∶1∶1
) = 1∶1∶1
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三11月阶段测化学卷(解析版) 题型:推断题
A、B、C、D、E是中学化学常见单质, X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系 (反应物和产物中的H2O已略去):
(1)Y的电子式为 ,构成E单质的元素在周期表中的位置 。
(2)反应②的离子方程式为 。
(3)足量C通入Y的溶液中可得到一种常见的消毒剂。在该消毒剂中通入少量CO2可得一种酸式盐,从酸性强弱角度请你写出得到的结论: 。
(4)①写出检验N中阳离子常用的试剂名称 ,N也可用来净水,请写 出相关离子方程式 。
出相关离子方程式 。
②H的溶液在空气中久置,会变浑浊,请写出相关离子方程式
(5)C可用来制取漂白粉,为测定漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为 (不考虑生成CaSO4):
静置。待完全反应后,用1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为 (保留到小数点后两位)。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上周考五化学试卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】
化合物H的分子中含有醛基和酯基,H可以用C和F在一定条件下合成(如图);
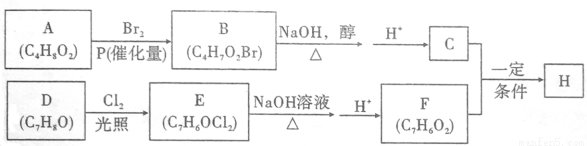
已知以下信息:
①A的核磁共振氢谱中有三组峰;且能与饱和碳酸氢钠溶液反应放出CO2。
②
③化合物D苯环上的一氯代物只有两种。
④通常同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
(1)A的化学名称_____________________;(系统命名法)
(2)B的结构简式为_____________________;
(3)D生成E的化学方程式为_____________________,该反应类型为___________;
(4)F的结构简式为______________;
(5)H在一定条件下反应生成高聚物的化学方程式为______________;
(6)F的同系物G比F相对分子质量大14,G的同分异构体中能同时满足如下条件:①苯环上只有两个取代基;不能使FeCl3溶液显色,共有_______种(不考虑立体异构)。G的一个同分异构体被酸性高锰酸钾溶液氧化后核磁共振氢谱为两组峰,且峰面积比为2:1,写出G的这种同分异构体的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上周考五化学试卷(解析版) 题型:选择题
(周考3滚动)氨是生产氨肥、尿素等物质的重要原料。电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法不正确的是
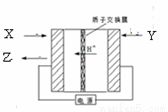
A.图中所示物质中,X为N,Y为H2,Z为NH3
B.Y参与的电极反应为H2+2e—=2H+
C.当有3g H+通过质子交换膜时,Z的体积为22.4L(标况)
D.反应过程中左边区域溶液pH逐渐降低
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一月考二化学卷(解析版) 题型:计算题
在铁和氧化铁的混合物 15 g 中加入150 mL 稀 H2SO4 放出氢气 1.68 L(标准状况下)。当反应停止后,铁与氧化铁均无剩余,且溶液中没有 Fe 3+存在。为了中和过量 H2SO4,并使 Fe 2+ 完全转化为 Fe(OH) 2沉淀,共耗用 3 mol·L-1 NaOH 溶液 200 mL。
(1) 写出溶液中反应的化学方程式:___________________;_____________________;______________________。
(2) 混合物中铁的质量为________,氧化铁的质量为________。
(3) 稀 H 2 SO 4的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
下列不能形成配位键的组合是
A.Ag+、NH3 B.BF3、NH3 C.Co3+、CO D.Ag+、H+
答
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com