
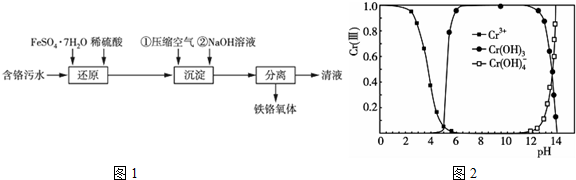
分析 含铬(主要成分是HCrO4-)污水,加入稀硫酸和硫酸亚铁,HCrO4-与亚铁离子发生氧化还原反应生成铁离子和铬离子,通入压缩空气既可以搅拌溶液,又可将部分亚铁离子氧化成铁离子,使溶液中铁离子和亚铁离子的物质的量之比为1:2,再加入氢氧化钠溶液形成铁铬氧体,若在加NaOH溶液之前通入的空气量过多,则溶液中亚铁离子的比例偏小,铁离子偏多,可以加入亚铁离子,或铁单质生成亚铁离子,根据图2所示可知,当溶液的pH在6.0~12时,铬以氢氧化铬的形式存在,可以除去溶液中的铬元素,再增大溶液的pH值时,铬元素以Cr(OH)4-形式存在,而溶解在水中,据此答题.
(1)还原过程中HCrO4-转化为Cr3+,亚铁离子被氧化成铁离子,根据得失电子守恒和电荷守恒配平并书写离子反应方程式,化合价升高后的产物为氧化产物;
(2)利用离心运动的机械叫做离心机,沸腾炉是为了增加反应物的接触面积,压缩空气通常采用压缩机进行压缩;
(3)通入压缩空气的目的是搅拌、将Fe2+氧化为Fe3+或调节Fe2+和Fe3+的比例,在加NaOH溶液之前通入的空气量不宜过多,若过多亚铁离子被氧化成铁离子偏多,据此分析解答;
(4)根据pH 的变化图分析氢氧化铬沉淀的PH,若pH过高,铬元素以Cr(OH)4-形式存在,而溶解在水中;
(5)Cr(OH)3的溶度积Ksp=c(Cr3+)•c(OH-)3,pH约为8,则c(OH-)=10-6mol/L,根据Ksp[Cr(OH)3]=6.3×10-31计算c(Cr3+).
解答 解:(1)HCrO4-与亚铁离子发生氧化还原反应生成铁离子和铬离子,根据得失电子守恒Fe2+、Fe3+,前系数都为3,结合电荷守恒,该反应的离子方程式为HCrO4-+3Fe2++7H+=Cr3++3Fe3++4H2O,亚铁离子被氧化成铁离子,所以反应产物Fe2(SO4)3为氧化产物,
故答案为:HCrO4-+3Fe2++7H+=Cr3++3Fe3++4H2O;Fe2(SO4)3;
(2)利用离心运动的机械叫做离心机,通常将悬浊液进行迅速沉淀采用离心机,沸腾炉是为了增加反应物的接触面积,压缩空气通常采用压缩机进行压缩,
故答案为:B;
(3)通入压缩空气既可以搅拌溶液,又可将部分亚铁离子氧化成铁离子,使溶液中铁离子和亚铁离子的物质的量之比为1:2,若通入的空气量过多,则溶液中亚铁离子的比例偏小,铁离子偏多,可以加入亚铁离子,或铁单质生成亚铁离子,故选AD,
故答案为:搅拌、将Fe2+氧化为Fe3+或调节Fe2+和Fe3+的比例;AD;
(4)根据图2所示可知,当溶液的pH在6.0~12时,铬以氢氧化铬的形式存在,可以除去溶液中的铬元素,再增大溶液的pH值时,Cr(OH)3+OH-=Cr(OH)4-,铬元素以Cr(OH)4-形式存在,而溶解在水中,
故答案为:6.0~12;Cr(OH)3+OH-=Cr(OH)4-;
(5)约为8,则c(OH-)=10-6mol/L,Ksp[Cr(OH)3]=6.3×10-31=c(Cr3+)•c(OH-)3,c(Cr3+)=$\frac{6.3×1{0}^{-31}}{(1{0}^{-6})^{3}}$=6.3×10-13mol/L,
故答案为:6.3×10-13mol/L.
点评 本题考查了污水处理以及磁性铁铬氧体的制备,涉及离子方程式书写、沉淀溶解平衡的计算等知识,注意控制溶液中铁离子和亚铁离子的比例是制备铁铬氧体的关键,答题时要注意抓住这一原理分析,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| X溶液 | 现象 | 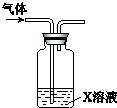 | |
| A | 紫色石蕊溶液 | 溶液先变红后褪色 | |
| B | 淀粉KI酸性溶液 | 溶液变为蓝色 | |
| C | 滴有KSCN的FeSO4溶液 | 溶液变为红色 | |
| D | 稀HNO3酸化的AgNO3溶液 | 有白色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图表示0.10 mol•L-1 NaOH溶液滴定20.00 mL 0.10 mol•L-1醋酸溶液的滴定曲线 | |
| B. |  图表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化 | |
| C. |  根据图所示可知:金刚石生成石墨为放热反应 | |
| D. |  图表示反应2SO2+O2?2SO3,t1时刻只小了的SO3的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2NaOH$\stackrel{加热加压}{→}$
+2NaOH$\stackrel{加热加压}{→}$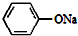 +NaCl+H2O
+NaCl+H2O
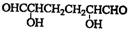 .
.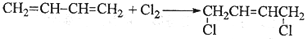 、
、 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
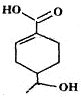
| A. | 分子中含有四种官能团 | |
| B. | 1mol该有机物完全燃烧消耗O2的物质的量为10mol | |
| C. | 能发生加成、取代、消去、水解等反应 | |
| D. | 相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生的气体的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
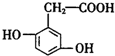 ,则下列说法错误的是( )
,则下列说法错误的是( )| A. | 1mol尿黑酸与足量的浓溴水反应,最多消耗3mol Br2 | |
| B. | 1mol尿黑酸最多能与4mol H2反应 | |
| C. | 尿黑酸分子中在同一平面上的碳原子至少有7个 | |
| D. | 尿黑酸可与碳酸氢钠溶液反应放出CO2,生成2.24LCO2(标况下)需要尿黑酸16.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
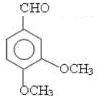 ;
; ;
;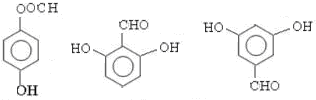 任意一种;(任写一种)
任意一种;(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同质子数相同的同种核素 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入少量CH3COONa固体 | B. | 通入少量氯化氢气体 | ||
| C. | 提高温度 | D. | 加入少量纯醋酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com