
【题目】(1)写出下列过程的化学方程式:
①CH3COOCH=CH2![]() A
A![]() B
B
聚合反应:______________________________________________
水解反应:_________________________________________________
②甘氨酸与盐酸反应:____________________________
(2)聚碳酸酯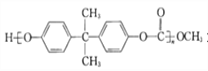 的透光率良好,可制作车、船、飞机的挡风玻璃等。原来合成聚碳酸酯的一种原料是有毒的光气(COCl2),现在改用绿色化学原料碳酸二甲酯
的透光率良好,可制作车、船、飞机的挡风玻璃等。原来合成聚碳酸酯的一种原料是有毒的光气(COCl2),现在改用绿色化学原料碳酸二甲酯![]() 与___________(填字母序号)缩合聚合而成。
与___________(填字母序号)缩合聚合而成。
a.二卤代物 b.二酚类 c.二醛类 d.二烯类
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
A.CH3Cl B.CH3CH(Br)CH3 C.(CH3)3C—CH2Cl D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界存在多种A的化合物,B原子核外电子由6种不同的运动状态,B与C可形成正四面体形分子,D的M能层没有空轨道且只有2个未成对电子。请回答下列问题:
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为________。
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有________个六元环;图2位在元素周期表中与B相邻的元素位置关系,B、G形成的晶胞结构如图3所示(其中“●”为B元素原子,“〇”为G元素原子),图中“●”点构成的堆积方式与图4中_____(填序号)所表示的堆积方式相同;图3的结构中,设晶胞边长为a cm,B原子直径为bcm,G原子直径为c cm,则该晶胞的空间利用率为_______(用含a、b、c的式子表示)。

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式_____(用化学式表示)。
(4)元素C的含氧酸中,酸性最强的是_________(写化学式),该酸根离子的立体构型为________。
(5)基态D原子的核外电子排布式为[Ar]_______;D形成的配合物D(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=______;由D一铝合金为原料可制得一种历史悠久、应用广泛的催化剂,其催化的i实例为: 化合物b中进行sp3杂化的原子有__________(填元素符号)。
化合物b中进行sp3杂化的原子有__________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量CO2气体通入硅酸钠溶液中,然后加热蒸干,再在高温下充分反应,最后所得的固体物质是
A. Na2SiO3 B. Na2CO3、Na2SiO3 C. Na2CO3、SiO2 D. SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列元素属于海水中的常量元素的是
①H ②O ③Na ④Cl ⑤Li⑥U ⑦Ca ⑧K ⑨Br ⑩F
A. ①②③④⑦⑧⑨⑩B. ③④⑦⑧⑨⑩
C. ①②③④⑥⑦⑧⑨⑩D. ③④⑥⑦⑧⑨⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的说法正确的是( )
A. 相邻的两个原子间可以形成化学键,多个原子间不可能形成化学键
B. 化合物中一定含有化学键,单质中也一定含有化学键
C. 相邻的两个或多个原子间的相互作用一定是化学键
D. 阴、阳离子之间的强相互作用也是化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国药学家屠呦呦因发现植物黄花蒿叶中含有抗疟疾的物质—青蒿素而荣获2015年诺贝尔奖。科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚。下列说法正确的是
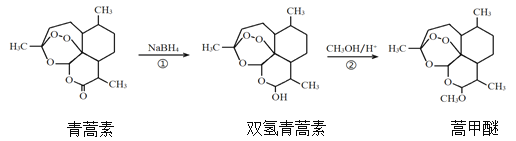
A.利用黄花蒿叶研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
B.①、②的反应类型分别为还原反应、酯化反应
C.双氢青蒿素在水中的溶解性大于青蒿素
D.双氢青蒿素与蒿甲醚组成上相差-CH2-,二者互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烷烃的叙述不正确的是( )
A. 烷烃中每个碳原子都形成4个共价单键
B. 正丁烷的4个碳原子可以在同一直线上
C. 甲烷、乙烷、丙烷的结构都只有一种
D. 任何烷烃分子不可能为平面结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com