
【题目】(1)烷烃A在同温、同压下蒸气的密度是H:的43倍,其分子式为____分子中含102个氢原子的烷烃的分子式是_____
(2)用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为__种。
(3)有机物 的正确命名为___________
的正确命名为___________
(4)立方烷 它的六氯代物有____种。
它的六氯代物有____种。
(5)  分子中最多有个____原子共面.
分子中最多有个____原子共面.
【答案】 C6H14 C50H102 6 3,3,4-三甲基已烷 3 23
【解析】烷烃的通式为:CnH2n+2,烷烃的相对分子量为:14n+2,(1)密度之比等于摩尔质量之比,就等于相等分子量之比,A的相对分子质量为:14n+2=43![]() =86,n=6,即该烷烃的分子式为C6H14;烷烃B的分子中含有102个氢原子,即2n+2=102,解得:n=50,所以B的分子式为C50H102;(2)式量为43的烷基为丙基,它有两种结构,连接到甲苯苯环上的时候又有三种位置,所以一共有6种产物;(3)有机物
=86,n=6,即该烷烃的分子式为C6H14;烷烃B的分子中含有102个氢原子,即2n+2=102,解得:n=50,所以B的分子式为C50H102;(2)式量为43的烷基为丙基,它有两种结构,连接到甲苯苯环上的时候又有三种位置,所以一共有6种产物;(3)有机物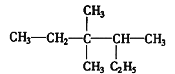 最长碳链为6个碳,第3个碳上有两个甲基,第4个碳上有一个甲基,正确命名为3,3,4-三甲基已烷;
最长碳链为6个碳,第3个碳上有两个甲基,第4个碳上有一个甲基,正确命名为3,3,4-三甲基已烷;
(4) 立方烷的同分异构体分别是:一条棱、面对角线、体对角线上的两个氢原子被氯原子代替,所以二氯代物的同分异构体有3种;分子中共含有8个H原子,则六氯代物与二氯代物的同分异构体数目相同,同分异构体数目为3;(5) 根据甲烷为正四面体结构,苯分子中12个原子共平面,则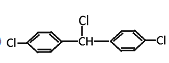 分子中若两个
分子中若两个![]() 旋转到同一面,则剩下
旋转到同一面,则剩下![]() 这里有两个原子不在同一平面上,故最多有23个原子在同一平面上。
这里有两个原子不在同一平面上,故最多有23个原子在同一平面上。


科目:高中化学 来源: 题型:
【题目】已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)![]() CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
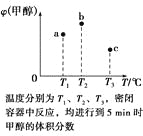
A. 正反应的ΔH>0
B. 反应进行到5 min时,b容器中v正=v逆
C. 减压可将b中的平衡状态转变成c中的平衡状态
D. 达到平衡时,a、b、c中CO的转化率为b>a>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、![]() 的混合物中加入100 mL浓度为
的混合物中加入100 mL浓度为![]() 的盐酸,二者恰好完全反应,放出224 mL的气体
的盐酸,二者恰好完全反应,放出224 mL的气体![]() 标准状况
标准状况![]() ,所得溶液中加入KSCN溶液后无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
,所得溶液中加入KSCN溶液后无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是![]()
![]()
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示表示物质X、Y、Z、W在一定条件下可以按照箭头一步转化。
序号 | X | Y | Z | W |
|
(1) | |||||
(2) |
|
| |||
(3) |
|
|
(1)X是金属单质,焰色反应呈黄色;Y的纯净物易潮解;Z可用于治疗胃酸过多;X在黄绿色的气体中燃烧可以产生白烟W(已知:电解熔融态的W可以得到X)。
X是:___________Y是:___________Z是:__________W是:__________(填写化学式)
(2)Z具有漂白性,但是不稳定,易分解产生含氯化合物。Z是:________(填写化学式)
(3)鉴别X、Y可以滴加___________溶液,前者出现血红色。(填写名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物异搏定合成路线中,其中的一步转化如下:
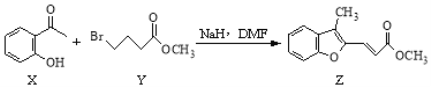
下列说法正确的是
A. Y的分子式为C5H9O2Br
B. X分子中所有原子在同一平面内
C. Z和足量H2加成后的分子中有5个手性碳原子
D. 等物质的量的X、Z分别与溴水反应,最多消耗Br2的物质的量之比1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.二甲醚(DME)-种清洁的替代燃料,不含硫,不会形成微粒,而且与汽油相比,排放的NO2更少,因此是优良的柴油机替代燃料。工业上利用一步法合成二甲醚的反应如下(复合催化剂为CuO/ZnO/Al203):2CO(g)+4H2(g) ![]() CH3OCH3(g)+H2O(g)△H=-204.7kJ/mol。
CH3OCH3(g)+H2O(g)△H=-204.7kJ/mol。
(1)600℃时,一步法合成二甲醚过程如下:

则△H2=____。
(2)以DME为燃料,氧气为氧化剂,在酸性电解质溶液中用惰性电极制成燃料电池,则通入氧气的电极是电源的____(填正、负)极,通DME的电极反应为
Ⅱ.2007年诺贝尔化学奖获得者格哈德·埃特尔建立了合成氨反应机制。T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ/mol(注:图中“吸”表示在催化剂表面的吸附)。请回答下列问题:
(1)合成氨反应的机理为

①________________________

(2)T=673K,合成氨反应的热化学方程式为______________
(3)液氨和水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为2NH3 ![]() NH4++ NH2一(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=____。
NH4++ NH2一(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=____。
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物。它易溶于水,溶液呈酸性,水解原理与NH4C1类似。写出盐酸肼第一步水解反应的离子方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氧化铁样品中含有少量的硫酸亚铁。某同学要测定其中铁元素的质量分数,设计了如下实验方案。

(1)操作Ⅰ中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有__________(填仪器名称)。
(2)反应①中加入足量H2O2溶液,反应的离子方程式:_______________________________。
(3)检验沉淀中![]() 是否洗涤干净的操作是_______________________________________。
是否洗涤干净的操作是_______________________________________。
(4)将沉淀加热,冷却至室温,用天平称量坩埚与加热后固体的总质量为b1g,再次加热并冷却至室温称其质量为b2g,若b1-b2=0.3,还应进行的操作是_____________________。
(5)坩埚的质量为42.6 g,最终坩埚与加热后的固体的总质量为45.8 g,则样品中铁元素的质量分数为________________。
(6)有同学认为上述方案的实验步骤太繁琐,他认为,只要将样品溶于水充分搅拌,加热、蒸干、灼烧称量即可测得样品中铁元素的质量分数,你认为他的这个方案是否可行?__________(填“可行”或“不可行”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素及其化合物的转化关系如下图所示:

回答下列问题:
(1)实验室常用下图装置制取并收集氨气,试管中发生反应的化学方程式是_____________。
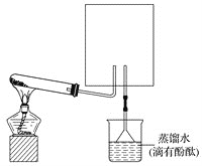
(2)上图中的方框内收集氨气的装置是________(填下图中的字母)。
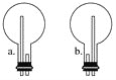
(3)用NH3制取NO的化学方程式是__________________。
(4)工业上将NO2通入Na2CO3溶液中进行吸收处理,完成相应的化学方程式:2NO2+Na2CO3===NaNO2+________+________,_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体 (H2C2O4)和浓硫酸混合缓慢加热时,可发生如下反应:H2C2O4 = CO2↑+CO↑+H2O 某课外活动小组的学生设计了如下实验装置,用来制取干燥纯净的 CO 气体,并用生成的 CO 气体还原 FexOy 制取铁粉。

(1)装置 B 的作用是_____。装置 E 中的现象是_________。装置 F 的作用是_________。
(2)装置 D 中玻璃管中发生反应的化学方程式为_____。
(3)若 FexOy 为 0.4g,生成的气体与过量澄清石灰水反应生成 0.75g 白色沉淀,则 FexOy 的化学式为_____。
(4)在实验开始时,点燃A、D 酒精灯的先后顺序是_____,实验完毕后,熄灭A、 D酒精灯的先后顺序是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com