
| A. | 加入少量W,逆反应速率增大 | |
| B. | 当容器中气体压强不变时,一定是n(X):n(Y):n(Z)=1:1:1 | |
| C. | 当容器中气体的平均相对分子质量不变时,一定是V(X):V(Y):V(Z)=1:1:1 | |
| D. | 加入X,上述反应的△H增大 |
分析 A.W为固体,少量改变量对反应无影响;
B.温度、体积一定,n与p成正比,压强不变时总物质的量不变;
C.始终存在反应速率之比等于化学计量数之比;
D.焓变与参加反应的物质的量无关.
解答 解:A.加入少量W,反应速率不变,平衡不移动,故A错误;
B.当容器中气体压强不变时,气体的总物质的量不变,不一定存在n(X):n(Y):n(Z)=1:1:1,与起始量、转化率有关,故B错误;
C.当容器中气体的平均相对分子质量不变时,由速率之比等于化学计量数之比,可知一定存在V(X):V(Y):V(Z)=1:1:1,故C正确;
D.加入X,上述反应的△H不变,故D错误;
故选C.
点评 本题考查化学平衡移动,为高频考点,把握体积不变时物质的量与压强的关系为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
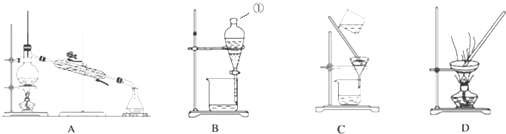
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它可使石蕊试液褪色 | |
| B. | 通入BaCl2溶液中,生成白色沉淀 | |
| C. | SO2通入氢氧化钠与酚酞的混合溶液中红色变浅直至褪去 | |
| D. | 等物质的量的Cl2和SO2通入品红溶液中,品红溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释后,醋酸的电离程度增大,溶液的导电性增强 | |
| B. | c(H+)=c(CH3COO-) | |
| C. | 加入少量醋酸钠固体后,恢复至室温,溶液中c(CH3COO-)•c(H+)/c(CH3COOH)不变 | |
| D. | 与等体积pH=12的NaOH溶液混合后,pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同体积和 pH 的盐酸和醋酸溶液,与足量锌粒生成气体不相同 | |
| B. | pH 相同的盐酸和醋酸溶液,加水稀释 100 倍后两溶液 pH 仍相同 | |
| C. | 中和 pH 与体积均相同的盐酸和醋酸溶液,消耗 NaOH 的物质的量相同 | |
| D. | 25℃,将 pH=5 的盐酸稀释 1000 倍后,溶液的 pH=8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com