
����Ŀ��ijС��ͬѧ��һ�������Ͻ�Ϊԭ�ϣ�ģ����صĹ�ҵ��������Ӧ������ͼ��ʾ�����ֲ������������ȥ������ش�
��1�������Ͻ���һ�ָߵ�����ܺϽ������й��Ʋ������ȷ����_____������ţ���
A.�����Ͻ�������������ڻ���Ƴ�
B.�����Ͻ���۵����������
C.�����Ͻ�Ӳ�ȸ��ڴ���
��2����Ӧ������Ԫ�ط�����Ӧ�����ӷ���ʽΪ ��
��3����Ӧ�ڵĻ�ѧ����ʽΪ ��
��4����Ӧ�۷���ʱ�۲쵽�������� ��
��5����Ӧ���е�CO2���˻���HCl��ԭ���� ��
��6����ֱ�ٳ�����A��B��һ����;�� ��
���𰸡�
��1��A,C
��2��Al3++4OH��=AlO2��+2H2O
��3��2Al+2NaOH+2H2O=2NaAlO2+3H2��
��4���Ȳ�����ɫ����,֮��Ѹ�ٱ�ɻ���ɫ����Ϊ���ɫ
��5���������Ȼ����ʹ���ɵ����������ܽ�
��6������ɫ����,ұ����
����������������1���������Ϸ����������Ͻ�������������ڻ���Ƴɣ���A��ȷ�������Ͻ���۵��������������B���������Ͻ�Ӳ�ȸ��ڴ�������C��ȷ����2����Ӧ�� �������������������������ƫ�����ƺ������ƣ����ӷ���ʽΪAl3++4OH��=AlO2��+2H2O����3����Ӧ������������������Һ��Ӧ����ƫ�����ƺ���������Ӧ��ѧ����ʽ��2Al+2NaOH+2H2O=2NaAlO2+3H2������4����Ӧ�� ����������������������Һ��Ӧ���ɰ�ɫ���������������������ƣ������������ױ����������ɺ��ɫ�����������������Ȳ�����ɫ������֮��Ѹ�ٱ�ɻ���ɫ����Ϊ���ɫ����5��ƫ�����������������̼��Ӧ������������������̼�����ƣ�ƫ�����������HCl��Ӧ�����Ȼ��������Է�Ӧ���е�CO2���˻���HCl����6������A����������������ɫ�������B������������������ұ������
��ֻ�������ᣬ������������ת������Σ�Ҳ�������������ƣ�ת���ƫ������
��1�����������Ʒ�Ӧ��Ĺ���������������������������������������ת����������������ڿ����б�������������������
��2������������ת�����������������������ת������Σ��������������ƣ���������ת������������������������������������������ƫ�����ƺ���������Һ������������ת���ɹ�����������������ת��������������Һ��NaAlO2�����������̼��Ӧ����������������������ת������������
��1���Ͻ��ص㣺����ɽ������۵�͡�Ӳ�ȸ�
��2����Ӧ�� �������������������������ƫ�����ƺ������ƣ����ӷ���ʽΪAl3++4OH��=AlO2��+2H2O
��3����Ӧ������������������Һ��Ӧ����ƫ�����ƺ���������Ӧ��ѧ����ʽ��2Al+2NaOH+2H2O=2NaAlO2+3H2��
��4����Ӧ�� ����������������������Һ��Ӧ���ɰ�ɫ���������������������ƣ������������ױ����������ɺ��ɫ�����������������Ȳ�����ɫ������֮��Ѹ�ٱ�ɻ���ɫ����Ϊ���ɫ
��5��ƫ�����������������̼��Ӧ������������������̼�����ƣ�ƫ�����������HCl��Ӧ�����Ȼ��������Է�Ӧ���е�CO2���˻���HCl
��6������A����������������ɫ�������B������������������ұ����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Q��R��T��X��Y��Z������ԭ���������������ǰ�����ڳ���Ԫ�أ��������Ϣ�����
Ԫ�� | �����Ϣ |
Q | Q�ĵ�����ʵ���ҳ��õĶ��Ե缫���� |
R | Rԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵ��� |
T | �����۵�Ԫ��T���⻯����ͨ���������һ��Һ�壬�� T����������Ϊ88.9% |
X | X�ǵ������ڵ縺������Ԫ�� |
Y | Ԫ��Yλ�����ڱ���10�� |
Z | Z����������Ϊ65��������Ϊ36�ĺ��� |
��1��ZԪ�ص�ԭ�ӻ�̬ʱ�ĵ����Ų�ʽ��
��2������������ȷ���� a��Q�������̬�⻯���R�������⻯���ȶ�
b��Q�ĺ�����һ����R�ĺ���������ǿ
c��R����̬�⻯����۵���ͬ��Ԫ���γɵ��⻯�������
d��R�ĵ�һ�����ܡ��縺�Զ���Q��
��3��Q��T���γ����ֳ���������ֱ��ʾΪQT��QT2 �� QT�����ЦҼ��м��ĸ�����Ϊ��QT2�����У�Qԭ�Ӳ�ȡ�ӻ���
��4��Ц����R2T����һ�����������й�������ΪR2T��QT2�������ƵĽṹ���ʵĿռ乹��Ϊ �� ��Ϊ������ԡ��Ǽ��ԡ������ӣ�
��5������Q��Y��þ����Ԫ�ص�ij�־�����г����ԣ��侧���ṹ��ͼ��ʾ���þ���Ļ�ѧʽΪ��������ÿ��þԭ����Χ��������������Yԭ�������� 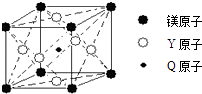
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������AG��ʾ��Һ����ȣ�acidity grade����AG�Ķ���ΪAG=lg[ ![]() ]��������ʵ��������0.01molL��1������������Һ�ζ�20.00mL0.01molL��1�Ĵ��ᣬ�ζ�������ͼ��ʾ������������ȷ���ǣ� ��
]��������ʵ��������0.01molL��1������������Һ�ζ�20.00mL0.01molL��1�Ĵ��ᣬ�ζ�������ͼ��ʾ������������ȷ���ǣ� �� 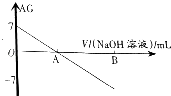
A.�����£�����ĵ��볣��ԼΪ10��5
B.A��ʱ��������������Һ�����Ϊ20.00mL
C.��B��Ϊ40mL��������Һ�У�c��H+��=c��CH3COO����+c��CH3COOH��
D.��Ӧ������һ�����ڣ�0.01molL��1+c��OH����=c��Na+��+c��CH3COOH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. �����������������Ҫ���������ʣ�����Ҫ���ˮ��
B. ��֬���������ʶ��ܹ�Ϊ�����ṩ����
C. �ϳ���ά���Ͻ𡢺ϳ����Ǻϳɲ���
D. ���˿ɽ���ˮ��Ӳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ũ�Ⱦ�Ϊ0.1molL��1��������Һ����Na2CO3����NaHCO3����HCl
��1����Һ���а����ʵ���Ũ���ɴ�С˳�����и���Һ�и�����Ũ����
��2����Һ���У�c��CO32����+c��HCO3����+c��H2CO3��= molL��1��
��3����10mL��Һ�ۼ�ˮϡ����100mL�����ʱ��Һ����ˮ�������c�� H+��=molL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�ѧ��ʶ������˵����ȷ���ǣ� ��
A. ijʳƷ��װ����һС�������������Ҫ�ɷ���CaCO3
B. �ӵ�ʳ���еġ��⡱ͨ��ָ�ⵥ��
C. ũҩ������Һ����ʢ��������������
D. �����ĸɵ��Ӧ�û��ռ��д���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β���ŷŵ�һ����̼����������������ѳ�Ϊ������Ⱦ����Ҫ��Դ���¹���������β���������¼�����ȫ��������������ʾ��ͼ�ش��й����⣺ 
��1����������������ʱ������N2��g��+O2��g��=2NO��g����H=+180kJmol��1 �� �������仯ʾ��ͼ���£� ![]()
��NO�е������ļ���ΪkJmol��1��
��2����ȼ�ȹ�С�ײ���CO���������������Ʒ�Ӧ2CO��g��=2C��s��+O2��g��������CO����Ⱦ���жϸ������Ƿ���У���˵��������
��3�����û���̿Ϳ�������ܴ���NOx�ķ�ӦΪ��xC��s��+2NOx��g��N2��g��+xCO2 ��g����H=��b kJmol��1 �� ��ʹNOx������Ч��ת��Ϊ��β���ŷţ����´�ʩ�����Ͽ��е�����
A.���������ܳ���
B.����β���ŷſ�
C.�����������¶�
D.���Ӻ��ʵĴ���
��4����װ�����漰�ķ�Ӧ֮һΪ��2NO��g��+2CO��g��N2��g��+2CO2��g���� 
��̽��������Ӧ��NO��ƽ��ת������ѹǿ���¶ȵĹ�ϵ���õ�ͼ2��ʾ�����ߣ���װ�ñȽ��ʺϵ��¶Ⱥ�ѹǿ����
�ڲ���ij�ͺ���������������������ָ������ˮ�µ͵������������ʱ��װ����CO��NO�ٷֺ�����ʱ��仯������ͼ3��ʾ����ǰ10s �ڣ�CO��NO�ٷֺ���û���Ա仯��ԭ������
���о���������ʹ�õ���������ʱ����������ȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ�������������ʵ�飺
ʵ���� | T��K�� | NO��ʼŨ�� | CO��ʼŨ�� | �����ıȱ������m2/g�� |
�� | 400 | 1.00��10��3 | 3.60��10��3 | 82 |
�� | 400 | 1.00��10��3 | 3.60��10��3 | 124 |
�� | 450 | 1.00��10��3 | 3.60��10��3 | 124 |
��������ͼ4������400Kʱ�÷�Ӧ��ƽ�ⳣ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪AΪӦ�ù㷺�Ľ������ʡ�B��Һ��dz��ɫ��C��Һ��ɫ��Ӧ����ɫ��C��Һ��ʹ��̪��Һ�ʺ�ɫ������������ͼ��ʾ���ת����
�Իش�
��1��д��B�Ļ�ѧʽ �� D�Ļ�ѧʽ��
��2��д����Eת���F�Ļ�ѧ����ʽ��
��3��д����G��Һ�м���A�����ӷ���ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����״���ṹ��ϩ������Bowtiediene������״�ͽṹ����ͼ��ʾ���йظ÷��ӵ�˵������ȷ����(����)
A.��ϩ���ķ���ʽΪC5H4
B.�÷�������̼ԭ����ͬһƽ��
C.1mol���л���������2molBr2�����ӳɷ�Ӧ
D.���以Ϊͬ���칹����ֻ��������������ֹһ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com