
(16分)碘元素的单质和化合物在现实生产生活中应用广泛。
(1)碘化钾(KI)是常用的还原剂。某研究性学习小组利用碘酸钾(KIO3)测定碘化钾的浓度。在10.00mL的KI溶液中逐滴滴入用硫酸酸化的 KIO3溶液,溶液颜色不再变化后,用Na2S2O3溶液滴定生成的I2(使用淀粉做指示剂),消耗0.2000mol·L-1 Na2S2O3溶液30.00mL。
滴定过程发生的离子方程式如下:2S2O32-+I2===S4O62-+2I-;
①写出本实验中碘酸钾和碘化钾反应的化学方程式,并标出电子转移的方向和数目:_______________________________________________________。
②滴定终点判断 ;
③测定的KI溶液浓度是 mol·L-1。
(2)探究酸性KIO3溶液的与KI溶液反应中KIO3浓度和温度对反应速率的影响,生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。
某同学设计实验如下表所示:
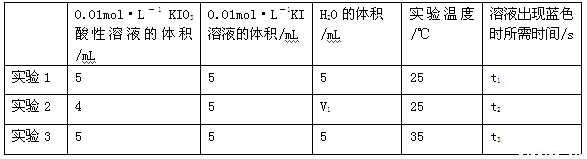
①由小到大比较t1、t2、t3的大小 ;表中V1= mL;
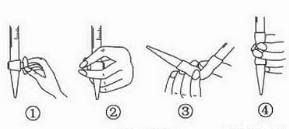
②用Na2S2O3标准溶液滴定生成的I2,滴定前排气泡时,应选用下图中的_________。
(1)①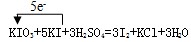 (用双线桥法表示亦可得分) (方程式2分,桥及标注1分)
(用双线桥法表示亦可得分) (方程式2分,桥及标注1分)
②当滴入最后一滴Na2S2O3溶液时,溶液恰好由蓝色变为无色且半分钟内不恢复原色;(3分);
③0.5000;(3分,写0.5给2分)
(2)①t3<t1<t2(3分); 6(2分)② ③ (2分)
试题分析:(1)①KIO3和KI在酸性条件下发生归中反应生成I2,其化学方程式及电子转移的情况如下: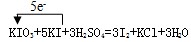
②碘酸钾和碘化钾反应生成的碘单质,加入淀粉显蓝色,用Na2S2O3溶液滴定生成的I2至终点时,溶液由蓝色变为无色,故滴定终点判断为:当滴入最后一滴Na2S2O3溶液时,溶液恰好由蓝色变为无色且半分钟内不恢复原色;③根据反应:KIO3+5KI+3H2SO4=3I2+KCl+3H2O和2S2O32-+I2===S4O62-+2I- 可知:5KI—3I2—6S2O32-,则KI溶液浓度为: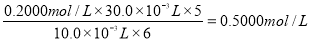 ;④ ③ (3分)。
;④ ③ (3分)。
(2)①根据表中信息可知:溶液总体积相等均为15 mL ,故V1=6 mL ,实验1与实验3相比,其他条件相同,温度较低,反应速率较慢,t3<t1,实验1与实验2相比,,其他条件相同,浓度较高,反应速率较快,t2<t1,则t3<t1<t2;②标准液Na2S2O3是强碱弱酸盐,其水溶液呈碱性,故只能用碱式滴定管,且碱式滴定管滴定前排气泡时应选如③图。
考点:考查氧化还原测定的应用、实验基本操作、化学计算。


科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:实验题
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
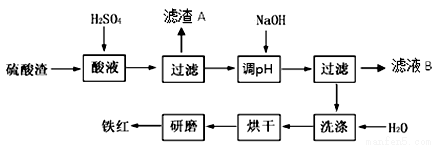
(1)硫酸渣的成分中属于两性氧化物的是 , 写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: ;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_________;(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)滤渣A的主要成分为 ,滤液B可以回收的物质有Na2SO4、MgSO4和___________;
(4)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为 (用最简分数表达式表示)。
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第二次调研考试化学试卷(解析版) 题型:选择题
X、Y、Z、W均为短周期主族元素,右图为周期表的一部分。W原子的最外层电子数是其电子层数的2倍。下列说法正确的是
| X |
| Y |
Z |
| W |
|
A.通常情况下,X元素只存在两种氧化物
B.Y元素气态氢化物的还原性最强
C.X元素的非金属性比Y元素非金属性强
D.W的最高价氧化物对应水化物的酸性比Z的强
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:实验题
(16分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
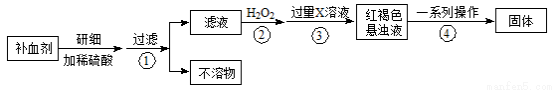
请回答下列问题:
(1)补血剂存放时间较长会氧化变质,对滤液中铁元素的存在形式提出如下假设:
假设1:只有Fe2+
假设2:只有Fe3+
假设3: 。
(2)如何证明步骤①滤液中含有Fe2+ 。
(3)步骤④中一系列处理的操作步骤: 、洗涤、灼烧、 、称量。
(4)该小组有些同学认为可用酸化的KMnO4溶液滴定进行Fe2+含量的测定。
①用离子方程式表示该滴定原理:____________________
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、量筒、药匙、胶头滴管外,还需 。
重复滴定三次,消耗1.00 mol/L KMnO4标准溶液体积分别为19.98 mL、20.00 mL、20.02mL,3次实验所用Fe2+溶液的体积为20.00 mL。请根据以上数据,再设计合理数据,完成下列实验过程的记录表格。(必须填满)
实验编号 | Fe2+溶液的 体积/mL |
|
|
|
1 | 20.00 |
|
|
|
2 | 20.00 |
|
|
|
3 | 20.00 |
|
|
|
③如何判断达到滴定终点:____________________________。
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
类推是学习和研究的重要思维方法。下列类推结论正确的是
| 化学事实 | 类推结论 |
A | Al在O2中燃烧生成Al2O3 | Fe在O2中燃烧也生成Fe2O3 |
B | pH=3的盐酸稀释1000倍后pH=6 | pH=6的盐酸稀释1000倍后pH=9 |
C | 用电解熔融MgCl2的方法冶炼金属镁 | 用电解熔融NaCl的方法制取金属钠 |
D | 将SO2通入BaCl2溶液中无沉淀生成 | 将SO2通入Ba(NO3)2溶液中也无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省增城市毕业班调研测试理科综合化学试卷(解析版) 题型:选择题
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如下图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。下列说法正确的是
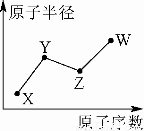
A.Y、Z、W处于同一周期
B.Y、W的最简单氢化物的水溶液能相互反应
C.非金属性:Y<Z
D.X、Z、W形成的化合物均为强酸
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三10月月考化学试卷(解析版) 题型:实验题
(16分)用芒硝(Na2SO4·10H2O)制备纯碱、铵明矾[NH4Al(SO4)2·12H2O]的生产工艺流程图如下所示:
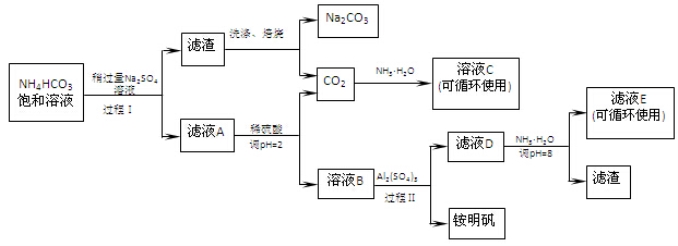
(1)溶液C中的溶质主要是 。
(2)铵明矾的溶液呈 性,铵明矾可用于净水,用离子方程式说明原理 。
(3)过程Ⅰ反应温度不能超过40℃,主要原因是 。
(4)运用化学平衡原理解释Na2SO4溶液稍过量的原因
(5)滤液E中溶质离子为
(6)写出工艺流程中焙烧的反应方程式
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
反应A(g) + B(g)  C(g) + D(g) 发生过程中的能量变化如下图,△H 表示反应的焓变。下列说法正确的是
C(g) + D(g) 发生过程中的能量变化如下图,△H 表示反应的焓变。下列说法正确的是
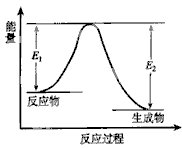
A.该反应为吸热反应
B.反应体系中加入催化剂,反应速率增大,E1减小,E2增大
C.反应体系中加入催化剂,反应速率增大,△H不变
D.反应达到平衡时,降低温度,A的转化率增大
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市高三上学期第二次模拟考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.S在纯氧中燃烧可生成SO3
B.用澄清石灰水可鉴别CO2和SO2
C.SO2能使KMnO4溶液褪色
D.CO2通入CaCl2溶液中能产生白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com