|
制取纯净的氯化铜晶体(CuCl2·2H2O)的生产过程如下:
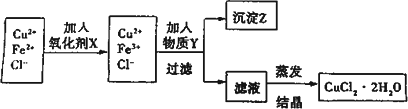
Ⅰ.将粗氧化铜(含少量Fe)溶解在足量的稀盐酸中,然后加热、过滤得到CuCl2(含少量FeCl2)溶液,经测定,溶液pH为2.
Ⅱ.对I中所得到的溶液按下列步骤进行提纯.
已知:
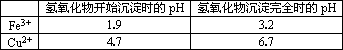
试回答下列问题:
|
(1) |
|
下列物质中,最适合作为氧化剂X的是
|
| [ ] |
A. |
KMnO4
|
B. |
K2Cr2O4
|
C. |
H2O2
|
D. |
NaClO
|
|
(2) |
|
①加紧入的物质Y是________.
②写出沉淀Z在水中的沉淀溶解平衡方程式:________.
|
|
(3) |
|
分离出沉淀Z,并将滤液蒸发,欲获得氯化铜晶体(CuCl2·2H2O),应采取的措施是________.
|
|
(4) |
|
①某同学利用反应:Cu+2H+ Cu2++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为________.(填“原电池”或“电解池”) Cu2++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为________.(填“原电池”或“电解池”)
②请你在下面方框中画出该同学设计的装置图,并指明电极材料和电解质溶液.

|
|
(5) |
|
已知一些难溶物的浓度积常数如下表:

某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的________除去它们.(选填序号)
①NaOH
②FeS
③Na2S
|
|
