
(12分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
肼—空气燃料电池放电时:
负极的电极反应式是 ;
正极的电极反应式是 。
(3)下图是一个电化学过程示意图。
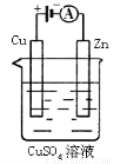
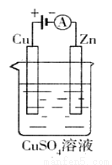
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
(1)N2H4(1)+O2(g) =N2(g)+2H2O(1);△H=―624kJ/mol
(2)N2H4+4OH-―4e-=4H2O+N2↑ O2+2H2O+4e-=4OH- ;
(3)①Cu2++2e-=Cu ②112
(4)ClO-+2NH3=N2H4+Cl-+H2O
【解析】
试题分析:
(1)热化学方程式的书写应注意物质的聚集状态,计量数和反应热数值之间的对应关系,正负号,ΔH的单位;32.0gN2H4为1mol,即N2H4(l)+O2(g) N2(g)+2H2O(l) ΔH=-624 kJ·mol-1;
N2(g)+2H2O(l) ΔH=-624 kJ·mol-1;
(2)空气燃料电池工作时,肼应该被氧化,化合价升高转变为氮气,在碱性条件下,H+转变成水,正极O2得电子转变成OH-;即正极:O2+2H2O+4e- 4OH-,负极:N2H4+4OH--4e-
4OH-,负极:N2H4+4OH--4e- 4H2O+N2↑;
4H2O+N2↑;
(3)①是电解池中的电镀池,所以Zn片上发生反应:Cu2++2e- Cu;
Cu;
由电子守恒可知,128gCu是2mol,对应1molO2,所以空气为22.4L×5=112 L。
(4)依据氧化还原反应的规律,得到ClO-+2NH3=N2H4+Cl-+H2O。
考点:考查热化学方程式和氧化还原反应、原电池、电解池
点评:本题综合考查了热化学方程式和氧化还原反应、原电池、电解池,考查学生的书写能力、思维能力及计算能力,难度较大。


科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学文试卷(解析版) 题型:?????
配制480mL1.0 mol·L-1NaNO2溶液,需称取溶质质量为
A.13.8g B.69g C.34.5g D.138g
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市东城区高一上学期期末考试化学试卷(解析版) 题型:实验题
(10分)探究SO2的性质。甲组同学将SO2分别通入下列3种溶液中。
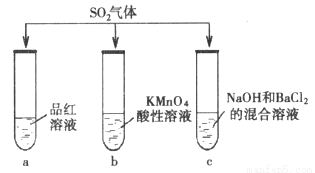
(1)试管a中观察到的现象是__________。
(2)试管b中观察到紫色褪去,说明SO2具有的性质是__________。
(3)试管c中产生了能溶于稀盐酸的白色沉淀,该白色沉淀是__________。
(4)乙组同学多做了一组实验,他们将SO2通入盛有1.0 mol/L Fe(NO3)3和BaCl2的混合溶液(已知1.0 mol/L Fe(NO3)3溶液中c(H+)=0.1 mol/L)的试管d中,得到了不溶于稀盐酸的白色沉淀。分析产生该白色沉淀的原因:
观点1:SO2与Fe3+反应
观点2:在酸性条件下SO2与 反应
反应
观点3:__________。
欲证明观点2,只需将试管d中Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是__________(填字母)。
a.0.1 mol/L稀硝酸
b.1.5 mol/L Ba(NO3)2和0.1 mol/L HNO3的混合溶液
c.6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市东城区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列反应既属于离子反应,又属于氧化还原反应的是
A.CaO+H2O= B.
B.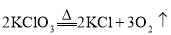
C. D.
D.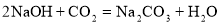
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市东城区高一上学期期末考试化学试卷(解析版) 题型:选择题
当光束通过下列分散系时,能观察到丁达尔效应的是
A.NaOH溶液 B.稀H2SO4 C.CuSO4溶液 D.Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二12月月考化学试卷(解析版) 题型:选择题
草酸是中强酸,草酸氢钾溶液呈酸性。在0.1 mol·L-1 KHC2O4溶液中,下列关系正确的是
①c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
②c(HC2O4-)+c(C2O42-)=0.1 mol·L-1
③c(C2O42-)>c(H2C2O4)
④c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
A.①② B.①④ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二12月月考化学试卷(解析版) 题型:选择题
把abcd四块金属片浸入稀硫酸中,用导线两两相连组成原电池若ab相连时,a为负极;cd相连时,电流由d到c;ac相连时,c极上产生大量气泡;bd相连时,b上产生大量气泡则四种金属的活动性顺序由强到弱的是
A.a>b>c>d B.a>c>d>b C.c>a>b>d D.b>d>c>a
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高一上学期第三次月考化学试卷(解析版) 题型:选择题
氯气与冷的氢氧化钠反应生成NaCl与NaClO,与热的氢氧化钠反应生成NaCl与NaClO3.一定温度下,氯气与氢氧化钠反应生成的NaClO与NaClO3的物质的量之比为2:3,求该反应氧化产物与还原产物的物质的量之比为
A、5/16 B、5/17 C、5/13 D、13/5
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列反应能用勒夏特列原理解释的是
A.煅烧粉碎的黄铁矿矿石有利于SO2的生成
B.硫酸生产中用98%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3
C.加入催化剂有利于氨的合成
D.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com