
因存在浓度差而产生电动势的电池称为浓差电池。利用如图所示装置进行实验,开始先闭合K2,断开Kl,一段时间后,再断开K2,闭合Kl,形成浓差电池,电流计指针偏转(Ag+浓度越大,氧化性越强)。下列说法不正确的是
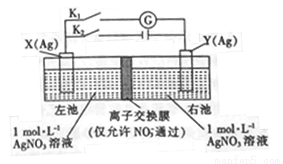
A. 闭合K2,断开Kl一段时间后,X电极质量增加
B. 闭合K2,断开Kl一段时间后,右池c(AgNO3)增大
C. 断开K2,闭合K1, X 电极发生氧化反应
D. 断开K2,闭合K1, NO3-从左池向右池移动
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
配制物质的量浓度为0.1mol•L-1的Na2CO3溶液100 mL时,下列操作正确的是
A. 用托盘天平称取1.06 g 无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 定容时,若仰视,则所配溶液的浓度将偏高
查看答案和解析>>
科目:高中化学 来源:2017届四川省成都市高三二诊模拟考试理综化学试卷(解析版) 题型:实验题
黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如下:

(1)黄铜矿中Cu 的化合价是______,反应I中65gFeC13 可氧化________mol CuFeS2。
(2)工业生产中的过滤操作多采用倾析法分离出固体物质,下列适合用倾析法的有______。
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)在反应Ⅱ中,计算NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3mol/L)可产生FeCO3沉淀时的最小Fe2+浓度是_________(己知FeCO3的Ksp=3.0×10-11)
(4)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式_________________。
(5)固体物质A的成分________(写名称)。
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红,写出相关的化学方程式:_______________。
(7)本流程中可实现循环使用的物质除了水外,还有_____________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省泰安市高三第一轮复习质量检测(一模)理科综合化学试卷(解析版) 题型:选择题
一种以NaBH4和H2O2为原料的新型电池的工作原理如图所示。下列说法错误的是
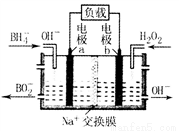
A. 电池的正极反应为H2O2+2e-==2OH-
B. 电池放电时Na+从a极区移向b极区
C. 电子从电极b经外电路流向电极a
D. b极室的输出液经处理后可输入a极室循环利用
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三第二次大联考理综化学试卷(解析版) 题型:简答题
三盐(3PbO·PbSO4·H2O)可用作聚氯乙烯的热稳定剂,200℃以上开始失去结晶水,不溶于水及有机溶剂。以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示。
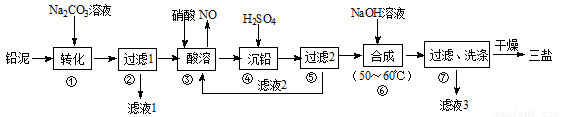
已知:PbSO4和PbCO3的溶解度和溶度积Ksp如下表。
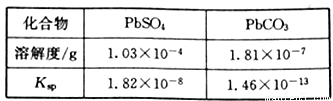
(1)步骤①转化的目的是_______,滤液1中的溶质为Na2CO3和_______(填化学式)。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是_________(任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为__________________。
(3)滤液2中可循环利用的溶质的化学式为_______。若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=______mol/L。
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是________________。
(5)步骤⑥合成三盐的化学方程式为____________,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为________。
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三下学期第二次质量监测理综化学试卷(解析版) 题型:简答题
M是一种重要材料的中间体,结构简式为:(CH3)2CHCOO 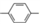 CHO。合成M的一种途径如下:
CHO。合成M的一种途径如下:
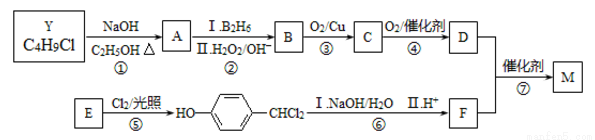
A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:① RCH=CH2 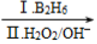 RCH2CH2OH
RCH2CH2OH
两个羟基连接在同一个碳原子上不稳定,易脱水;
请回答下列问题:
(1)若Y的核磁共振氢谱只有1种峰,则Y的结构简式为____________ 。
(2)A的名称是____________,由B生成C的反应类型为____________ 。
(3)M中的官能团有____________ (填官能团名称)。
(4)步骤⑥中反应I的化学方程式为 ___________________________。
(5)步骤⑦的化学反应方程式是_____________________________。
(6)D的同分异构体中,能在碱性条件下水解的有_______种(不包括立体异构),其中能发生银镜反应的同分异构体的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三下学期第二次质量监测理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. PH=6的溶液一定显酸性
B. 25℃时,0.1mol/L的NaHB溶液呈酸性,说明H2B为强酸
C. NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用
D. 0.1mol/LCH3COOH溶液与0.05mol/LNaOH溶液等体积混合,所得溶液中:2c(Na+)═c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:选择题
下列叙述正确的是
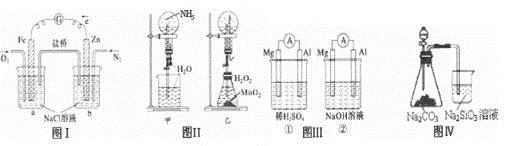
A. 图I装置中通入N2和O2的作用是相同的
B. 图Ⅱ中甲、乙两装置产生喷泉的原理一样
C. 图Ⅲ①装置中镁片是原电池的负极;②装置中镁片是原电池的正极
D. 图Ⅳ分液漏斗盛硝酸能证明非金属性N>C>Si,盛硫酸能证明非金属性S>C>Si
查看答案和解析>>
科目:高中化学 来源:2017届四川省乐山市高三第二次调查研究考试理科综合化学试卷(解析版) 题型:填空题
[化学——选修3:物质结构与性质]
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________。
(4)由A、B、C形成的离子CAB?与AC2互为等电子体,则CAB?的结构式为___________。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为___________。
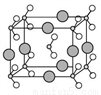
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________。
(7)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com