
| A. | 0.025mol•L-1•s-1 | B. | 0.0125mol•L-1•s-1 | ||
| C. | 0.05mol•L-1•s-1 | D. | 0.1mol•L-1•s-1 |
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化性A->B- | B. | 还原性 A->B- | C. | 氧化性 A>B | D. | 还原性A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
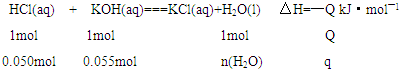
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液变蓝 | B. | Na浮在水面上并熔化成小球 | ||
| C. | Na在水面上游动 | D. | 有H2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
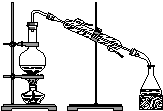 | 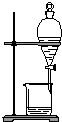 |  | 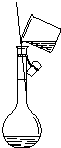 |
| A用海水制蒸馏水 | B将碘水中的碘单质与水直接分离 | C除去Fe(OH)3胶体中的FeCl3 | D稀释浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合金都一定是两种金属熔合而成 | |
| B. | 涂料属于高分子材料,不属于合成材料 | |
| C. | 水泥与水搅拌静之后会凝固变硬,这是水泥的水硬性 | |
| D. | 我国的陶都和瓷都都是宜兴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com