
| 1 | ||||||||||||||||||
| 2 | D | B | A | |||||||||||||||
| 3 | J | I | H | C | G | F | E | |||||||||||
| 4 | L | K | M | N | ||||||||||||||
分析 (1)元素周期表中,化学性质最活泼的金属在左下角,化学性质越活泼则金属性越强,非金属性最强的在右上角,溴单质在常温下是液体;
(2)根据元素的非金属性越强其对应的氢化物越稳定来回答;
(3)同周期元素原子半径从左到右逐渐减小;
(4)I、H位于同周期,从左向右金属性减弱,元素最高价氧化物对应水化物的碱性减弱.
解答 解:根据元素周期表中元素的分布知识,可以知道:A是F,B是O,C是P,D是C,F是Cl,E是Br,G是S,H是P,I是Mg,J是Na,K是Ca,L是K,M是Mn,N是Br,
(1)元素周期表中,从上到下金属的活泼性逐渐增强,从右到左金属活泼性逐渐增强,所以化学性质最活泼的金属在左下角,应该是K,化学性质越活泼则金属性越强,所以金属性最强的也是K,稀有气体元素化学性质是最稳定的,即Ar化学性质是最稳定,元素周期表中,从下到上元素的非金属性逐渐增强,从左到右非金属性逐渐增强,所以非金属性最强的在右上角,应该是F,溴单质在常温下是液体,M处于中间10列,应为过渡元素,故答案为:Ar;K;F;Br;M;
(2)元素周期表中,从下到上元素的非金属性逐渐增强,从左到右非金属性逐渐增强,所以非金属性顺序是Cl>O>P,元素的非金属性越强其对应的氢化物越稳定,则稳定性顺序为:HCl>H2O>PH3,故答案为:PH3;
(3)同周期元素原子半径从左到右逐渐减小,所以原子半径最小的是Cl,故答案为:Cl;
(4)I、H位于同周期,从左向右金属性减弱,元素最高价氧化物对应水化物的碱性减弱,金属性Mg>Al,对应最高价氧化物的水化物为碱,且碱性Mg(OH)2>Al(OH)3,故答案为:Mg(OH)2;Al(OH)3;Mg(OH)2>Al(OH)3.
点评 本题考查元素周期表及其应用,把握元素在周期表的位置推断元素及元素的性质为解答的关键,注意非金属性、金属性的比较,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清的石灰水与稀盐酸反应:OH-+H+=H2O | |
| B. | 氢氧化钡溶液与稀硫酸反应:Ba2++OH-+SO${\;}_{4}^{2-}$+H+=BaSO4↓+H2O | |
| C. | 氧化铜与盐酸反应:O2-+2H+=H2O | |
| D. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉与水蒸气反应过程中应先加热制备水蒸气,再加热铁粉 | |
| B. | 侯氏制碱法中向饱和食盐水中应先通入足量NH3,再通入CO2 | |
| C. | 向包有Na2O2的脱脂棉花上滴水以观察到“生火”现象,滴的水应该尽量多 | |
| D. | Fe(OH)3胶体制备实验中向沸水滴入FeCl3溶液应是饱和溶液,并且滴入的用量仅为几滴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、Al3+ | B. | HCl、H2S、Ar | C. | H2O、OH-、Na+ | D. | NH4+、Na+、F- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 适当升高温度 | B. | 加入适量的水 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入浓度较大的硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | CH3C(CH3)2CH2CH2CH(CH2CH3)CH3 的系统命名为:2,2,5-三甲基庚烷 | |
| C. | 羟基的电子式: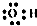 | |
| D. | CCl4的电子式: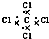 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com