
【题目】现有如下两个反应:
a.![]() ;
;
b.![]()
(1)反应__________(填字母)不能设计成原电池,原因是____________________。
(2)根据上述能设计成原电池的反应,画出简单的原电池实验装置图____________________,并注明电极材料和电解质溶液。写出正极的电极反应式________________________。
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】化学与生活、人类生产、社会可持续发展密切相关,下列说法正确的是( )
A.合成材料、光伏材料和复合材料都是新型无机非金属材料
B.晋代![]() 抱扑子
抱扑子![]() 中记载有“丹砂烧之成水银,积变又还成丹砂”是指加热时丹砂
中记载有“丹砂烧之成水银,积变又还成丹砂”是指加热时丹砂![]() 熔融成液态,遇冷又重新凝结成HgS晶体
熔融成液态,遇冷又重新凝结成HgS晶体
C.煤的干馏是化学变化,煤的气化、液化和石油的分馏都是物理变化
D.![]() 本草经集注
本草经集注![]() 中记载了区别硝石
中记载了区别硝石![]() 和朴硝
和朴硝![]() 的方法:“以火烧之,紫青烟起,乃真硝石也”这是运用了“焰色反应”的原理
的方法:“以火烧之,紫青烟起,乃真硝石也”这是运用了“焰色反应”的原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应C(s)+H2O(g)![]() CO(g)+H2(g),ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
CO(g)+H2(g),ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
A.升高温度B.增大水蒸气浓度
C.加入大量CD.降低压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5 表示。有关说法正确的是

A. 该装置为原电池,b为原电池的负极
B. 中间室Na+移向右室,Cl-移向左室,a极区溶液的pH减小
C. 当左室有4.48L(标准状况下)CO2生成时,右室产生的N2为0.8mol
D. b电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl4是制备钛及其化合物的重要中间体,可利用下列装置在实验室制备TiCl4(夹持装置略去): TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
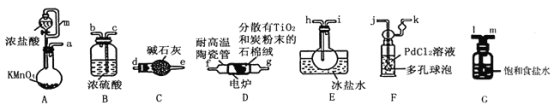
已知:①PdCl2溶液捕获CO时生成Pd单质;②相关数据如下表:
化合物 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 |
TiCl4 | -25 | 136 | 1.5 | 能溶于有机溶剂:遇水分解生成难溶于水的物质 |
CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
回答下列问题:
(1)装置A中连通管的作用是______;装置E中使用冰盐水浴的目的是_____________________。
(2)按照气流由左到右的方向,上述装置合理的连接顺序为____________________ (填仪器接口字母);根据完整的实验装置进行实验,实验步骤如下:_____________; 装入药品;向装置A烧瓶中滴加适量浓盐酸,当观察到_________时,加热装置D中陶瓷管;装置E烧瓶中的液体量不再增加时,停止加热,充分冷却。
(3)装置C的作用为___________________。
(4)装置F中发生反应的化学方程式为________________________。
(5)制得的TiCl4中常含有少量CCl4, 从混合液体中分离出TiCl4的操作名称为_______________。
(6)利用如图所示装置测定产品纯度:称取w g TiCl4产品进行实验,向安全漏斗中加入适量蒸馏水,待四氯化钛充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,用氢氧化钠溶液调节至中性,滴加几滴0.1 molL-1的K2CrO4溶液作指示剂,用cmol L-1 AgNO3标准溶液滴定至终点( Ag2CrO4为红棕色沉淀,可指示滴定终点),重复滴定两次,平均消耗标准溶液V mL。
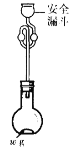
已知:TiCl4 +(2+x)H2O=TiO2xH2O↓+4HCl
①安全漏斗在本实验中的作用除加水外,还有___________。
②根据上述数据计算该产品的纯度为__________。(用含w、c和V的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.隔绝空气高温加热生物质,通过热化学转换可产生可燃性气体
B.光![]() 电转换的途径必定是发生了化学反应
电转换的途径必定是发生了化学反应
C.开发太阳能、氢能、核能、天然气等新能源可以减少霾的产生
D.植物秸秆发酵制沼气是在有氧条件下进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离
B.电解质越弱,则其溶液的导电能力就越差
C.在白色ZnS沉淀上滴![]() 溶液,沉淀变黑,说明相同条件下溶解度CuS比ZnS更小
溶液,沉淀变黑,说明相同条件下溶解度CuS比ZnS更小
D.加热NaR溶液时,溶液的pH变小,证明HR为弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿![]() 主要成分为
主要成分为![]() 、
、![]() 、
、![]() ,少量
,少量![]() 和金属硫酸盐
和金属硫酸盐![]() 为原料,生产氧化铝并获得
为原料,生产氧化铝并获得![]() 的部分工艺流程如下:
的部分工艺流程如下:

![]() 粉碎高硫铝土矿石的目的是______。
粉碎高硫铝土矿石的目的是______。
![]() 焙烧时发生氧化还原反应:______
焙烧时发生氧化还原反应:______![]() ______
______![]() ______
______![]() ______
______![]() ,配平该方程式。
,配平该方程式。
![]() 碱浸时发生反应的化学方程式为______。
碱浸时发生反应的化学方程式为______。
![]() 过滤后向滤液中通入过量的
过滤后向滤液中通入过量的![]() 气体,反应的离子方程式为______。
气体,反应的离子方程式为______。
![]() “过滤”得到的滤渣中含有大量的
“过滤”得到的滤渣中含有大量的![]() 与
与![]() 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成![]() 和
和![]() ,理论上完全反应消耗的
,理论上完全反应消耗的![]() :
:![]() ______。
______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列操作、现象,所得结论正确的是![]()
选项 | 操作 | 现象 | 结论 |
A | 向25mL冷水和沸水中分别滴入5滴 | 前者为黄色. 后者为红褐色 | 温度升高, 程度增大 |
B | NaOH的乙醇溶液与溴乙烷共热,产生的气体通入 酸性高锰酸钾溶液中 | 溶液褪色 | 产生的气体为乙烯 |
C | 铜铝合金加入一定量稀硝酸中,有金属剩余,再加稀硫酸 | 剩余金属质量减小 | 铝与稀硫酸反应使 剩余金属质量减小 |
D | 盛有 | 气体变为无色 |
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com