
【题目】可逆反应:![]() 在恒容容器中进行,达到平衡状态的标志是( )
在恒容容器中进行,达到平衡状态的标志是( )
①单位时间内生成![]() 的同时生成
的同时生成![]()
②单位时间内生成![]() 的同时生成
的同时生成![]()
③用![]() 、
、![]() 、
、![]() 的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态
的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.①④⑥B.②③⑤C.①③④D.①②③④⑤⑥
【答案】A
【解析】
①单位时间内生成![]() 的同时生成
的同时生成![]() ,说明反应v(正)=v(逆),达到平衡状态,①正确;
,说明反应v(正)=v(逆),达到平衡状态,①正确;
②单位时间内生成![]() 的同时生成
的同时生成![]() ,这是必然的,无论反应是否达到平衡状态都满足,
,这是必然的,无论反应是否达到平衡状态都满足,![]() ,不能说明达到平衡状态,②错误;
,不能说明达到平衡状态,②错误;
③反应中必然满足![]() 和
和![]() ,但是只有
,但是只有![]() 才平衡,当用
才平衡,当用![]() 、
、![]() 、
、![]() 的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态,可能已经平衡,也可能没有平衡,与各物质的初始浓度及转化率有关,③错误;
的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态,可能已经平衡,也可能没有平衡,与各物质的初始浓度及转化率有关,③错误;
④混合气体的颜色不再改变,说明NO2气体的浓度不变,达到平衡状态,④正确;
⑤无论反应是否达到平衡状态,混合气体的质量不变,容器的体积不变,所以混合气体的密度不变,不能说明达到平衡状态,⑤错误;
⑥反应前后气体的化学计量数之和不相等,反应过程中,混合气体的物质的量一直变化,又因为气体质量不变,所以混合气体的平均相对分子质量一直不变,当其不再变化时,说明达到平衡状态,⑥正确;
答案选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验 编号 | HA物质的量 浓度(mol/L) | NaOH物质的量 浓度(mol/L) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)从①组情况分析,HA是__________(填“强酸”或“弱酸”)。
(2)②组情况表明,c__________(填“>”、“<”或“=”)0.2 mol/L。混合液中离子浓度c(A-)与c(Na+)的大小关系是__________。
(3)从③组实验结果分析,说明HA的电离程度__________(填“>”、“<”或“=”)NaA的水解程度,该混合溶液中离子浓度由大到小的顺序是__________________。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。写出该混合溶液中下列算式的精确结果(不能近似计算)。
c(Na+)-c(A-)=________mol·L-1;
c(OH-)-c(HA)=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国不同能源发电量占比如下。下列说法错误的是![]()
水电 | 火电 | 核电 | 风电 | 太阳能发电 |
|
|
|
|
|
A.燃煤发电能量转换过程为化学能![]() 电能
电能![]() 热能
热能![]() 机械能
机械能
B.水能、风能、核能及太阳能都属于清洁能源
C.大幅度增大水电、核电、风电及太阳能发电比例,有利于环境保护
D.水能、煤、风能及太阳能发电过程中均没有新核素生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。减少CO2排放是一项重要课题。
(1)碳酸二甲酯(CH3OCOOCH3,简称DMC)是一种应用前景广泛的新材料,用甲醇、CO、CO2在常压、70~120 ℃和催化剂条件下合成DMC。
已知:①CO(g) +1/2O2(g) === CO2(g) ΔH1=-283.0 kJ·mol-1
②H2O(l)===H2O(g) ΔH2=+44.0 kJ·mol-1
③2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g) ΔH3=-15.5 kJ·mol-1
CH3OCOOCH3(g)+H2O(g) ΔH3=-15.5 kJ·mol-1
则2CH3OH(g)+CO(g)+1/2O2(g) ![]() CH3OCOOCH3(g)+H2O(l) ΔH=________。
CH3OCOOCH3(g)+H2O(l) ΔH=________。
(2)在2L的密闭容器中通入2 mol CH3OH和1 mol CO2,按反应③合成DMC,一定条件下,平衡时CO2的转化率如图所示,则:

①A点的平衡常数为_________________
②v(A)、v(B)、v(C)由快到慢的顺序为__________________;
③下列能说明在此条件下反应达到平衡状态的是________。
A.2v正(CH3OH)=v逆(CO2)
B.CH3OH与CO2的物质的量之比保持不变
C.恒容条件,容器内气体的密度保持不变
D.各组分的物质的量分数保持不变
(3)CO2经催化加氢可以生成低碳烃,主要有以下两个竞争反应:
反应Ⅰ:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
反应Ⅱ:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
为分析催化剂对反应的选择性,在1 L密闭容器中充入1 mol CO2和2 mol H2,测得有关物质的物质的量随温度变化如图所示。

①该催化剂在较低温度时主要选择________(填“反应Ⅰ”或“反应Ⅱ”)。
②用惰性电极电解强酸性的二氧化碳水溶液可得到乙烯,其原理如图所示。b电极上的电极反应式为________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不发生消去反应的是( )
①![]() ②
②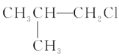 ③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤
③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A.①③⑥B.②③⑤C.全部D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:

相关反应的热化学方程式为:
反应I:SO2(g) + I2(g) + 2H2O(l) === 2HI(aq) + H2SO4(aq) ΔH1 =﹣213 kJ·mol-1
反应II:H2SO4(aq) === SO2(g) + H2O(l) + ![]() O2(g) ΔH2 = +327 kJ·mol-1
O2(g) ΔH2 = +327 kJ·mol-1
反应III:2HI(aq) === H2(g) + I2(g) ΔH3 = +172 kJ·mol-1
下列说法不正确的是:
A. 该过程实现了太阳能到化学能的转化
B. SO2和I2对总反应起到了催化剂的作用
C. 总反应的热化学方程式为:2H2O(l) === 2H2 (g)+O2(g) ΔH = +286 kJ·mol-1
D. 该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组用如下图所示装置制备、收集Cl2,并进行性质验证实验(夹持装置略去)。下列说法正确的是( )

A. 用![]() 和浓盐酸制备
和浓盐酸制备![]() 时,只选
时,只选![]()
B. ![]() 用于
用于![]() 收集时,a为进气口
收集时,a为进气口
C. ![]() 中加入NaBr溶液和
中加入NaBr溶液和![]() ,通入
,通入![]() 反应后振荡、静置,下层溶液呈橙红色
反应后振荡、静置,下层溶液呈橙红色
D. ![]() 中通入
中通入![]() 使品红溶液褪色后,取出溶液加热可恢复红色
使品红溶液褪色后,取出溶液加热可恢复红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com