
| A. | NaHCO3、MgCl2 | B. | NH4HCO3、AlCl3 | C. | (NH4)2 CO3、BaCl2 | D. | NH4 HCO3、MgCl2 |
分析 ①取少量样品加入足量水溶解;再加入足量氢氧化钠溶液(微热),产生白色沉淀并有气泡冒出,则气体为氨气,一定含铵盐,沉淀可能为不溶性碱;
②取少量样品加入足量稀盐酸有气泡产生,振荡后固体完全溶解,气体为二氧化碳,一定含碳酸根离子或碳酸氢根离子,以此来解答.
解答 解:A.NaHCO3、MgCl2的混合物与NaOH不反应生成氨气,故A不选;
B.NH4HCO3、AlCl3的混合物与足量NaOH不生成沉淀,故B不选;
C.(NH4)2 CO3、BaCl2的混合物溶于水反应生成沉淀,再加NaOH不生成沉淀,故C不选;
D.NH4 HCO3、MgCl2的混合物与NaOH反应生成氨气和氢氧化镁,与盐酸反应生成二氧化碳,故D选;
故选D.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应与现象为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
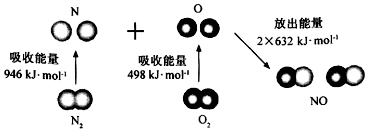
| A. | 直观看,该反应中反应物所具有的总能量低于生成物所具有的总能量 | |
| B. | 2 mol气态氧原子结合生成O2(g)时,能放出498 KJ能量 | |
| C. | 断裂1 mol NO分子中的化学键,需要吸收632KJ能量 | |
| D. | 该反应的热化学方程式为:N2+O2═2NO△H=+180KJ/mol. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ⑨ | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为8的氮原子:${\;}_{8}^{15}$N | |
| B. | 次氯酸的电子式: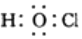 | |
| C. | PCl5分子的每个原子都满足8电子稳定结构 | |
| D. | 用电子式表示NaCl的形成过程: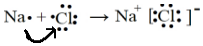 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑥ | B. | ①②④⑤ | C. | ①③⑥ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 溶液温度降低主要是因为NH4HCO3溶解吸热造成的 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 反应的热化学方程式为:NH4HCO3+HCl→NH4Cl+CO2↑+H2O-Q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4-甲基-3-丙基戊烷 | B. | 3-异丙基己烷 | ||
| C. | 2-甲基-3-丙基戊烷 | D. | 2-甲基-3-乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质溶液中加入Na2SO4可使其变性 | |
| B. | 蔗糖水解生成互为同分异构体的葡萄糖和果糖 | |
| C. | 顺-2一丁烯和反-2-丁烯的加氢产物不同 | |
| D. | 石油的分馏和煤的于馏均属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com