
1 1 |
2 1 |
 和
和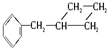
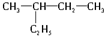 和
和 
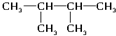 和
和 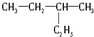
1 1 |
2 1 |
 和
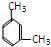
和 均含有苯环,属于芳香烃;
均含有苯环,属于芳香烃;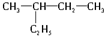 和
和  分子式相同,结构相同,为同一种物质;属于脂肪烃;
分子式相同,结构相同,为同一种物质;属于脂肪烃;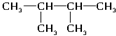 和
和  分子式相同,结构不同,存在碳链异构,互为同分异构体;属于脂肪烃;
分子式相同,结构不同,存在碳链异构,互为同分异构体;属于脂肪烃;

科目:高中化学 来源: 题型:
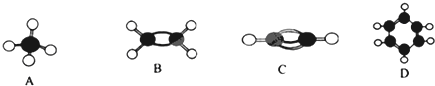
| A、A的二氯取代物只有一种,说明A为立体结构 |
| B、B不能使酸性高锰酸钾溶液褪色 |
| C、C中的碳氢质量比为6:1 |
| D、D能使溴水因反应而褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:
如图是实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
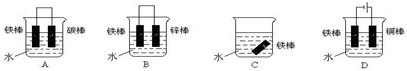
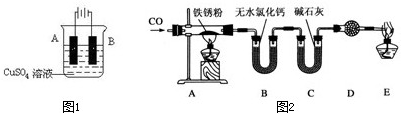
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com