
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
① 缓慢向烧瓶中通入过量混合气进行“浸锰”操作,主要反应原理为:
SO2+ H2O = H2SO3 ; MnO2+ H2SO3 = MnSO4+ H2O
(铁浸出后,过量的SO2 会将Fe3+还原为Fe2+)
② 向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末。
③ 再用Na2CO3溶液调节pH为3.5左右,过滤。
④ 调节滤液pH为6.5~7.2 ,加入NH4HCO3 ,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。回答下例问题:
(1)步骤②中加入一定量纯MnO2粉末的主要作用是将Fe2+氧化为Fe3+ ,将过量的SO2氧化除去,相应反应的离子方程式为 。
(2)查阅表1,步骤③中调pH为3.5时沉淀的主要成分是 。
表1:生成相应氢氧化物的pH
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
(3)步骤③中所得的滤液中含有Cu2+,可添加过量的难溶电解质MnS除去Cu2+,经过滤,得到纯净的MnSO4。用平衡移动原理解释加入MnS的作用_________________。
(4)④中加入NH4HCO3 后发生反应的离子方程式是____________________。
(5)检验④中沉淀是否洗涤干净的方法是 。
(6)现有常温下的四种溶液:
①0.1mol·L-1 NH4Cl溶液
②0.1mol·L-1 NH4Cl和0.1mol·L-1 NH3·H2O的混合溶液(显碱性)
③0.1mol·L-1 NH3·H2O
④0.1mol·L-1 NH4Cl和0.1mol·L-1 HCl
下例说法正确的有 (填字母序号)
A. NH4+离子浓度从大到小的顺序为②>④>①>③
B.溶液的pH从大到小的顺序为③>①>②>④
C.溶液中的离子总浓度从大到小的顺序为④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气脱硫是控制二氧化硫污染的主要技术手段。
(1)利用海水脱硫是一种有效的方法,其工艺 流程如图所示:
流程如图所示:
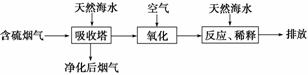
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示:
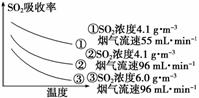
①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是________(填序号)。
A.降低通入含硫烟气的温度
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的离子方程式:__________________________________________________________
________________________________________________________________________。
③该小组采用如图装置在实验室测定烟气中SO2的体积分数(假设实验在标准状况下进行)。

上述装置连接的顺序是原料气→________(填a、b、c、d、e)。下列试剂中(浓度、体积一定),可以用来代替试管中的碘淀粉溶液的是________(填编号)。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
(2)石灰石石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙及鼓入的空气反应生成石膏(CaSO4·2H2O)。写出该反应的化学方程式:________________________________________________________________________
___________________________________________________ _____________________。
_____________________。
某电厂用煤300 t(煤中含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则可生产石膏________ t。
答案 (1)①ABD ②2H2SO3+O2===4H++2SO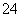
③c→d→b→a→e AC
(2)2CaCO3+2SO2+O2+4H2O===2(CaSO4·2H2O)+2CO2 38.7
查看答案和解析>>
科目:高中化学 来源: 题型:
中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据。这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法。下列说法中正确的是
A.正是氢键的存在,冰能浮在水面上
B.氢键是自然界中最重要、存在最广泛的化学键之一
C.由于氢键的存在,沸点:HCl>HBr>HI>HF
D.由于氢键的存在,水分子变的更稳定了
查看答案和解析>>
科目:高中化学 来源: 题型:
已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生如下反应:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
甲、乙两个实验小组欲探究影响化学反应速率的因素,设计实验方案如下(实验中所用KMnO4溶液均已酸化)
(1)甲组:通过测定单位时问内生成CO2气体体积的量来比较化学反应速率,实验装置如图,实验时分液漏斗中A溶液一次性加入,A、B的成分见下表:
| 序号 | A溶液 | B溶液 |
| ① | 2mL0.1 mol·L-1 H2C2O4溶液 | 4mL0.01 mol·L-1 KMnO4溶液 |
| ② | 2mL0.2 mol·L-1 H2C2O4溶液 | 4mL0.01 mol·L-1 KMnO4溶液 |
| ③ | 2mL0.2 mol·L-1 H2C2O4溶液 | 4mL0.01 mol·L-1 KMnO4溶液 少量MnSO4(催化剂) |
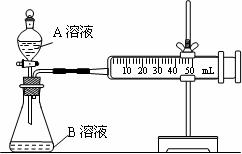
该实验探究的是 因素对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是 (填实验序号)。
(2)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率。取两支试管各加入2 mL 0.1 mol·L-1H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol·L-1 KMnO4溶液。将四支试管分成两组(每组各有一支盛有H2C2O4溶液和KMnO4溶液),一组放入冷水中,另一组放入热水中,一段时间后,分别混合并振荡,记录溶液褪色所需时间。
该实验试图探究 因素对化学反应速率的影响,但该组同学始终没有看到溶液完全褪色,其原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置能达到实验目的有(夹持仪器未画出) ( )
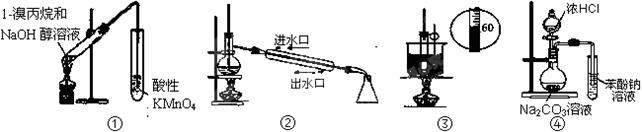
A.①装置用于检验1-溴丙烷消去产物 B.②装置用于石油的分馏
C.③装置用于实验室制硝基苯 D.④装置可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列物质的说法,正确的是( )

A.三者含有的官能团的种类相同 B.乙和丙中的-OH性质相同
C.甲和乙互为同分异构体 D.甲和丙互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
电化学在日常生活中用途广泛,图①是镁—次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O===Cl-+Mg(OH)2,图②是Cr2O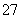 工业废水的处理。下列说法正确的是( )
工业废水的处理。下列说法正确的是( )
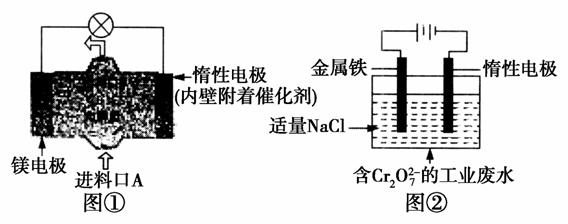
A.图②中Cr2O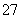 向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3被除去
向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3被除去
B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生
C.图①中发生的还原反应是:Mg2++ClO-+H2O+2e-===Cl-+Mg(OH)2↓
D.若图①中3.6 g镁溶解产生的电量用以图②废水处理,则理论可产生10.7 g氢氧化铁沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com