
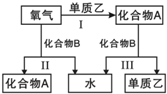
 A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题:
A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题: ;其水溶液呈碱性的原因是NH3+H20
;其水溶液呈碱性的原因是NH3+H20 NH4++OH-(用离子方程式表示).
NH4++OH-(用离子方程式表示).分析 (1)A、B是中学化学常见的化合物,它们各由两种元素组成,乙为元素R组成的单质,反应Ⅰ、Ⅱ为有氧气参加的反应,应为氧化还原反应,反应Ⅲ由化合物A、B反应生成单质,也应为氧化还原反应;
(2)元素R与氧同主族,则R为硫元素,硫的非金属性弱于氧,根据元素周期律判断;
(3)若化合物B常温下为气体,其水溶液呈碱性,则B为NH3,根据转化关系可知,A为NO,乙为N2,据此答题.
解答 解:(1)A、B是中学化学常见的化合物,它们各由两种元素组成,乙为元素R组成的单质,反应Ⅰ、Ⅱ为有氧气参加的反应,应为氧化还原反应,反应Ⅲ由化合物A、B反应生成单质,也应为氧化还原反应,所以属于氧化还原反应的有Ⅰ、Ⅱ、Ⅲ,共3个,
故答案为:3;
(2)元素R与氧同主族,则R为硫元素,硫的非金属性弱于氧,根据元素周期律可知,能说明S与氧的非金属性相对强弱的有,还原性:H2R>H2O、稳定性:H2R<H2O,
故答案为:A、C;
(3)若化合物B常温下为气体,其水溶液呈碱性,则B为NH3,根据转化关系可知,A为NO,乙为N2,
①化合物B的电子式为 ;其水溶液呈碱性的原因是氨水电离产生氢氧根离子,离子方程式为NH3+H20
;其水溶液呈碱性的原因是氨水电离产生氢氧根离子,离子方程式为NH3+H20 NH4++OH-,
NH4++OH-,
故答案为: ;NH3+H20
;NH3+H20 NH4++OH-;
NH4++OH-;
②化合物NH3与O2组成燃料电池(氢氧化钾溶液为电解质溶液),电池负极为氨气发生氧化反应生成氮气和水,电极反应式为2NH3-6e-+6OH-=N2+6H2O,
故答案为:2NH3-6e-+6OH-=N2+6H2O;
③当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为△H1和△H2,根据盖斯定律,将反应反应(Ⅰ-Ⅱ)×$\frac{4}{5}$可得反应Ⅰ的热化学方程式为N2(g)+O2(g)=2NO(g)△H=0.8(△H1-△H2),
故答案为:N2(g)+O2(g)=2NO(g)△H=0.8(△H1-△H2).
点评 本题考查了无机物转化关系的分析推断,依据化学反应类型,结合物质性质和相互转化关系分析判断是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
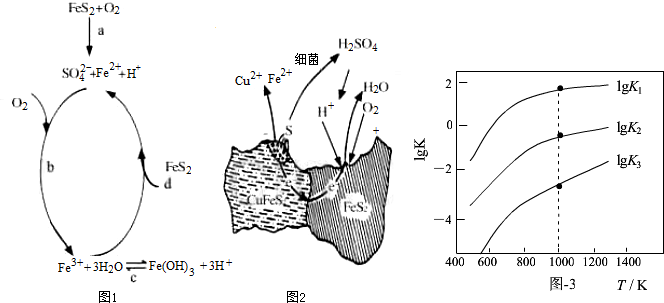
| 相关反应 | 反应热 | 平衡常数K |
| FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| $\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$Fe(s)+H2S(g) | △H2 | K2 |
| FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
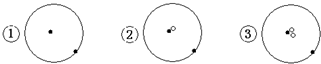
 表示质子或电子,
表示质子或电子, 表示中子,则下列有关的叙述正确的是( )
表示中子,则下列有关的叙述正确的是( )| A. | ①②③是三种化学性质不同的粒子 | B. | ①②③具有相同的质量数 | ||
| C. | ①②③为同素异形体 | D. | ①②③互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾霾是一种自然现象,对人体健康影响不大 | |
| B. | PM2.5是指大气中直径小于或等于2.5μm的颗粒物 | |
| C. | 大气中SO2含量的增加会导致温室效应加剧 | |
| D. | 酸雨是pH小于7的雨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁及其化合物在国民经济的发展中起着重要作用.
铁及其化合物在国民经济的发展中起着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳和环氧丙烷在催化剂作用下可生成一种可降解的高聚物 | |
| B. | 化石燃料的燃烧和含硫金属矿石的冶炼等都是造成SO2污染的重要原因 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 氟氯烃的大量使用会破坏臭氧层,火箭、导弹将大量废气排放到高空,也会加速臭氧分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Q的最高价氧化物对应的水化物酸性比W的强 | |
| B. | 化合物W2Q2中,各原子最外层均达8电子结构 | |
| C. | 工业上通过电解Z与Q形成的化合物制备Z单质 | |
| D. | Y单质与X的气态氢化物可发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①中仅发生一个反应 | |
| B. | Fe3+能催化H2O2的分解 | |
| C. | 反应过程中溶液pH不断减小 | |
| D. | FeSO4与等物质的量的H2O2恰好反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 1 mol•L-1盐酸中含有nA个HCl分子 | |
| B. | 32g O2与O3的混合物含有2nA个氧原子 | |
| C. | 1L 1 mol•L-1CuCl2溶液中含有nA个Cu2+ | |
| D. | 1mol Na与足量Cl2反应,转移2nA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com