
【题目】下列说法正确的是( )
A.石油液化气的主要成份为甲烷
B.煤的干馏可分离出煤中含有的煤焦油
C.石油的分馏和食盐水的蒸馏原理上是相似的
D.石油经过分馏得到的汽油是纯净物
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.少量金属钠加到冷水中:Na+2H2O═Na++2OH﹣+H2↑
B.NaHCO3溶液中滴加少量Ca(OH)2溶液:Ca2++OH﹣+HCO ![]() ═CaCO3↓+H2O
═CaCO3↓+H2O
C.硫酸铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO ![]() +4NH
+4NH ![]() +2H2O
+2H2O
D.将2 mol/L? AlCl3溶液和7 mol/L? NaOH溶液等体积混合:2Al3++7OH﹣═Al(OH)3↓+AlO ![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施中,不能增大化学反应速率的的是
A.Zn与稀硫酸反应制取H2时,加入蒸馏水
B.Al在O2中燃烧生成Al2O3时,用铝粉替代铝片
C.CaCO3与稀盐酸反应生成CO2时,适当升高温度
D.用KClO3固体分解制取O2时,固体中添加少量MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( ) 
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液中羟基和羧基均能电离出氢离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C6H14的各种同分异构体中所含甲基数和它的一氯取代物的数目分别是( )
A.2个甲基,能生成4种一氯代物
B.4个甲基,能生成1种一氯代物
C.3个甲基,能生成5种一氯代物
D.4个甲基,能生成4种一氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某纯碱试样中含有 NaCl 杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
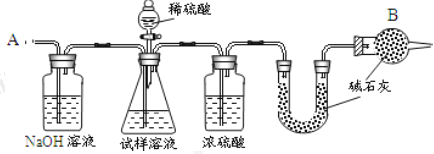
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将 a g 试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的 U 形管的质量,得到 b g;
④从分液漏斗滴入 6 molL-1的硫酸,直到不再产生气体时为止;
⑤从导管 A 处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的 U 型管的质量,得到 c g;
⑦重复步骤⑤和⑥的操作,直到 U 型管的质量基本不变,为 d g;
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明_________________。
(2)装置中干燥管 B 的作用是______________________。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________(填偏高、偏低或不变)。
(4)步骤⑤的目的是__________________________。
(5)步骤⑦的目的是__________________________。
(6)该试样中纯碱的质量分数的计算式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用如图所示装置进行探究实验.以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色. 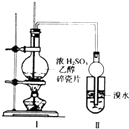
(1)写出该实验中生成乙烯的化学方程式:
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是 .
A.乙烯与溴水易发生取代反应
B.使溴水褪色的物质,未必是加成反应
C.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察后认为:
试管中另一现象可证明反应中有乙烯生成,这个现象是 . 为验证这一反应是加成而不是取代,可用PH试纸来测试反应后溶液的酸性,理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的氮肥,合成原理为:N2(g)+3H2(g) ![]() 2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
(1)写出平衡常数K的表达式 , 如果降低温度,该反应K值 , 化学反应速率 , N2的转化率(填“增大”、“减小”或“不变”).
(2)在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题: 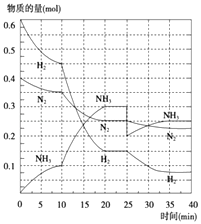
①10min内以NH3表示的平均反应速率: .
②在10~20min内,NH3浓度变化的原因可能是
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
③第1次达到平衡的时间为: , 第2次达到平衡的时间为:;
④在反应进行至25min时,曲线发生变化的原因
A.缩小容器体积 B.降低温度 C.分离了部分NH3
达第二次平衡时,新平衡的平衡常数K2K1 ,
(填“大于”、“小于”或“等于”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com