
【题目】下列有机方程式书写正确的是
A.苯酚钠溶液中通入少量二氧化碳:![]() +CO2+H2O→
+CO2+H2O→![]() +HCO3-
+HCO3-
B.甲烷与氯气的取代反应:CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
C.用苯制硝基苯:![]() +HO—NO2
+HO—NO2![]()
![]() +H2O
+H2O
D.苯乙酮与足量氢气加成: ![]()
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.食醋除水垢:![]()
B.稀硝酸中加入少量亚硫酸钠:![]()
C.处理工业废水时Cr(Ⅵ)的转化:![]()
D.用酸性KMnO4测定草酸溶液浓度:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Fe3+、Fe2+性质实验的说法错误的是( )
A.用如图装置可以制备沉淀Fe(OH)2
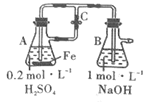
B.配制FeCl3溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度
C.向FeCl2溶液中加入少量铁粉是为了防止Fe2+被氧化
D.FeCl3溶液中滴加KSCN溶液会生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间的化学反应,反应产物一定为纯净物的是
A.CH3CH3+Cl2![]()
B.CH3-CH=CH-CH3+Br2
C.CH2=CH-CH2-CH3+HCl![]()
D.CH3-CH=CH2+H2O![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-。下列说法不正确的是
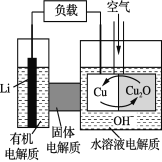
A. 放电时,Li+透过固体电解质向Cu极移动
B. 通空气时,铜被腐蚀,产生Cu2O
C. 放电时,正极的电极反应式为:Cu2O+2H+ +2 e- ===2Cu+H2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳等17种“分子”改变过人类的世界。
(1)铁原子在基态时,价层电子排布式为___。
(2)硝酸钾中NO3-的空间构型为___。
(3)1molCO2分子中含有σ键的数目为___。乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是___。
(4)6-氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有___。
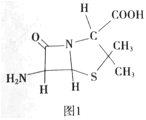
(5)铁和氨气在640℃可发生置换反应,产物之-的晶胞结构如图2所示,写出该反应的化学方程式___。
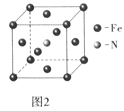
(6)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各微粒的相对位置。如图是CaF2的晶胞,其中原子坐标参数A处为(0,0,0);B处为(![]() ,
,![]() ,0);C处为(1,1,1)。则D处微粒的坐标参数为___。
,0);C处为(1,1,1)。则D处微粒的坐标参数为___。
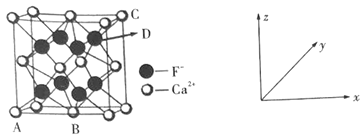
②晶胞参数:描述晶胞的大小和形状。已知CaF2晶体的密度为ρg·cm-3,则晶胞参数a为___pm(设NA为阿伏加德罗常数的值,用含ρ、NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家运用穿山甲的鳞片特征,制作出具有自我恢复性的防弹衣,具有如此神奇功能的是聚对苯二甲酰对苯二胺(G)。其合成路线如下:
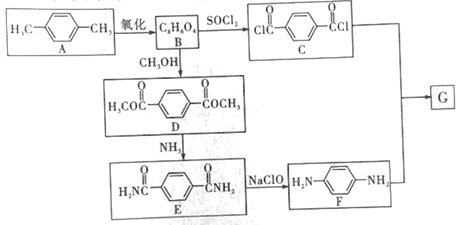
回答下列问题:
(1)A的化学名称为___。
(2)B中含有的官能团名称为___,B→C的反应类型为___。
(3)B→D的化学反应方程式为___。
(4)G的结构简式为___。
(5)芳香化合物H是B的同分异构体,符合下列条件的H的结构共有___种(不考虑立体异构),其中核磁共振氢谱有四组峰的结构简式为___。
①能与NaHCO3溶液反应产生CO2;②能发生银镜反应
(6)参照上述合成路线,设计以![]() 为原料(其他试剂任选),制备
为原料(其他试剂任选),制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(C21H20O6)在临床医学上具有预防肿瘤的作用,其合成路线如下,其中反应③中反应物的原子利用率为100%。
已知:Ⅰ. ![]()
![]()
![]() +H2O
+H2O
Ⅱ. ![]()
![]()
![]() +CO2
+CO2
Ⅲ. ![]() +
+![]()
![]()
![]() +H2O
+H2O
请回答下列问题:
(1) B中含有的官能团名称是____________。
(2)反应①的化学方程式是____________。 反应④的化学方程式是____________。
(3) F的结构简式是____________。
(4) E的同分异构体中,同时符合下列两个条件的共有__________种,其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为__________。
①苯环上的一取代物只有2种;
②1mol该物质与足量NaOH溶液反应时,反应消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯![]() ,熔点:
,熔点:![]() ,沸点:
,沸点:![]() 为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。是有机物合成中的重要试剂,常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置如图所示
为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。是有机物合成中的重要试剂,常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置如图所示![]() 其中III、IV中均为浓硫酸
其中III、IV中均为浓硫酸![]() :
:
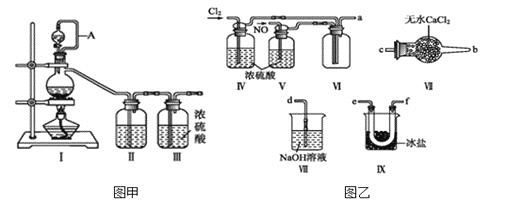
(1)用图甲中装置制备纯净干燥的原料气,补充下表中所缺少的药品。
| 装置Ⅰ | 装置Ⅱ | |
| 烧瓶中 | 分液漏斗中 | |
制备纯净 |
| 浓盐酸 |
|
制备纯净NO | Cu | 稀硝酸 |
|
(2)将制得的NO和![]() 通入图乙对应装置制备NOCl。
通入图乙对应装置制备NOCl。
![]() 装置连接顺序为
装置连接顺序为![]() ________
________![]() 按气流自左向右方向,用小写字母表示
按气流自左向右方向,用小写字母表示![]() 。
。
![]() 装置Ⅳ、Ⅴ除可进一步干燥NO、
装置Ⅳ、Ⅴ除可进一步干燥NO、![]() 外,还可以通过观察气泡的多少调节两种气体的流速。
外,还可以通过观察气泡的多少调节两种气体的流速。
![]() 有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、
有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、![]() 通入装置Ⅴ中,你同意此观点吗?_______
通入装置Ⅴ中,你同意此观点吗?_______![]() 填“同意”或“不同意”
填“同意”或“不同意”![]() ,原因是___________。
,原因是___________。
![]() 实验开始的时候,先通入氯气,再通入NO,原因为________________________。
实验开始的时候,先通入氯气,再通入NO,原因为________________________。
(3)有人认为多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置 ______;
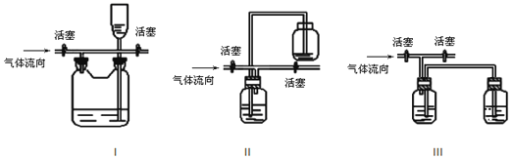
(4)装置Ⅶ吸收尾气时,NOCl发生反应的化学方程式为_______________________。
(5)有人认为装置Ⅶ中氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,因此在装置Ⅶ氢氧化钠溶液中加入高锰酸钾,反应产生黑色沉淀,写出该反应的离子方程式:__________________________________。
(6)制得的NOCl中可能含有少量![]() 杂质,为测定产品纯度进行如下实验:称取
杂质,为测定产品纯度进行如下实验:称取![]() 样品溶于
样品溶于![]() 溶液中,加入几滴
溶液中,加入几滴![]() 溶液作指示剂,用足量硝酸酸化的
溶液作指示剂,用足量硝酸酸化的![]() 溶液滴定至产生砖红色沉淀,消耗
溶液滴定至产生砖红色沉淀,消耗![]() 溶液
溶液![]() 。则该样品的纯度为__________
。则该样品的纯度为__________![]() 保留1位小数
保留1位小数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com