
| A、升高温度 |
| B、增大反应物浓度 |
| C、使用催化剂 |
| D、减小压强 |
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
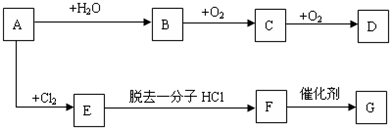
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、都是置换反应 |
| B、①中TiO2作氧化剂 |
| C、每生成1mol金属Ti,②中转移电子数为2NA |
| D、②中氩气作保护气,可防止金属Ti被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子、原子、离子都是构成物的粒子 |
| B、由同种元素组成的物质不一定是纯净物 |
| C、含有氧元素的化合物称为氧化物 |
| D、含有羟基的有机物不一定属于醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Ag+、Cl- |
| B、Cu2+、NO3-、Na+、OH- |
| C、Ba2+、NH4+、NO3-、SO42- |
| D、Al3+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com