
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B、平衡时,其他条件不变,增加CH4的浓度,氮氧化物的转化率减小 |
| C、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
| D、单位时间内消耗CH4和N2的物质的量比为1:2时,反应达到平衡 |


科目:高中化学 来源: 题型:
 溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法错误的是( )
溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法错误的是( )| A、温度升高时溴酸银溶解速度加快 |
| B、溴酸银的溶解是放热过程 |
| C、60℃时,溴酸银的Ksp约等于6×10-4 |
| D、常温下溴酸银微溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
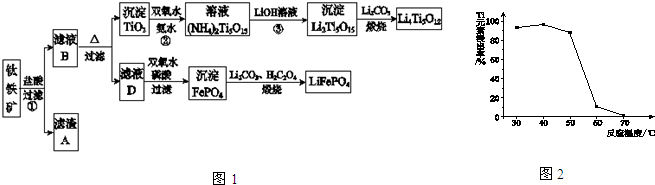
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:3 |
| C、1:2 | D、3:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Ba2+、Fe3+、NO3-,通入SO2气体 |
| B、Ca2+、Cl-、K+、H+,通入CO2气体 |
| C、AlO2-、Na+、Br-、SO42-,通入CO2气体 |
| D、HCO3-、Na+、I-、HS-,加入AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不含NO-3,可能含Fe3+ |
| B、含有NO3-、Cl-、I- |
| C、含I-,但不能确定是否含Cl- |
| D、含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2既是氧化产物又是还原产物 |
| B、氧化产物与还原产物物质的量之比为1:2 |
| C、联氨是氧化剂 |
| D、氧化剂与还原剂物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
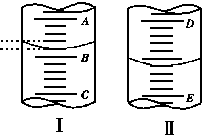 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol.L-1 盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 液体体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 氨碱法 | 联合制碱法 | ||
| A | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
| B | 可能的副产物 | 氯化钙 | 氯化铵 |
| C | 循环物质 | 氨气、二氧化碳 | 氯化钠 |
| D | 评价 | 原料易得;设备复杂;能耗高 | 原料利用率高;废弃物少 |
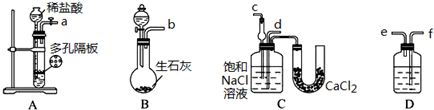
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com