
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是( )
A. 足量锌与一定量浓H2SO4反应生成0.5mol气体,反应中转移的电子数为NA
B. 1L 0.1mol/L的CH3COOH溶液中含有H+的数目约为0.1 NA
C. 电解精炼铜(粗铜中含有锌、铁、银等杂质),电路中有2NA个电子通过时,阴极增重64g
D. 常温常压下,1.8 g甲基(-CD3)中含有的电子数为0.9NA
【答案】B
【解析】浓硫酸与锌反应的方程式![]() =
=![]() ↑
↑![]() ,从方程式可以看出
,从方程式可以看出![]() 锌生成
锌生成![]() 二氧化硫气体,随着硫酸的消耗和水的生成,硫酸变稀,就会发生锌与稀硫酸反应,
二氧化硫气体,随着硫酸的消耗和水的生成,硫酸变稀,就会发生锌与稀硫酸反应,![]() ↑,从方程式可以看出
↑,从方程式可以看出![]() 锌生成
锌生成![]() 氢气,所以锌无论与浓硫酸反应还是与稀硫酸反应,如果生成气体为0.5 mol,转移电子数为NA;A正确;CH3COOH属于弱电解质,不能完全电离,所以1L 0.1mol/L的CH3COOH溶液中含有H+的数目小于0.1 NA,B错误;阴极极反应为:Cu2++2e-=Cu,当电路中有2NA个电子通过时,阴极增重64g,C正确;1mol甲基(-CD3)含有电子数为6+3×1=9NA,1.8 g甲基(-CD3)的量为0.1mol,所含有的电子数为0.9NA,D正确;正确选项:B。
氢气,所以锌无论与浓硫酸反应还是与稀硫酸反应,如果生成气体为0.5 mol,转移电子数为NA;A正确;CH3COOH属于弱电解质,不能完全电离,所以1L 0.1mol/L的CH3COOH溶液中含有H+的数目小于0.1 NA,B错误;阴极极反应为:Cu2++2e-=Cu,当电路中有2NA个电子通过时,阴极增重64g,C正确;1mol甲基(-CD3)含有电子数为6+3×1=9NA,1.8 g甲基(-CD3)的量为0.1mol,所含有的电子数为0.9NA,D正确;正确选项:B。


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】某元素R的阳离子是RN+ , 核外共有x个电子,其质量数为A,则R核内中子数为( )
A.A﹣X+N
B.A﹣X﹣N
C.A+X+N
D.A﹣N+X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料,制取氧化钴的流程如下:
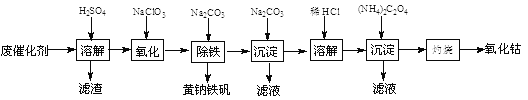
(1)溶解:溶解后过滤,将滤渣洗涤2~3次,滤渣的主要成分是________。(填化学式)
(2)氧化:加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,其离子方程式是________________。
已知:铁氰化钾化学式为K3[Fe(CN)6];亚铁氰化钾化学式为K4[Fe(CN)6]·3H2O。
3Fe2++ 2[Fe(CN)6]3- = Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++ 3[Fe(CN)6 ]4- = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是__________________________________________。(可供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(3)除铁:加入适量的Na2CO3调节酸度,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式:______________________________________。
(4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2·3Co(OH)2],沉淀需洗涤,洗涤的操作是_______________________。
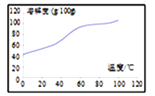
(5)溶解:CoCl2的溶解度曲线如图所示。向碱式碳酸钴中加入足量稀盐酸,边加热边搅拌至完全溶解后,需趁热过滤,其原因是___________________________。
(6)三氧化铁是一种重要的化合物,可以用来腐蚀电路板。常温下,某腐蚀废液中含有0.5 molL-1 Fe3+ 和0.26 molL-1 Cu2+,欲使Fe3+完全沉淀[c(Fe3+)<4×10-5 molL-1时完全沉淀]而Cu2+不沉淀,则需控制溶液 pH的范围为_________________。 {KspCu(OH)2]=2.6×10-19 ;KspFe(OH)3]=4×10-38}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是( )
A. 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+===Fe2+ + 2Fe3+ + 4H2O
B. Na2O2 加入H218O 中:2Na2O2 + 2H2l8O ===4Na+ + 4OH-+ 18O2↑
C. 水玻璃中通入过量二氧化碳:Na2SiO3 +CO2 + H2O===2Na+ +CO32- + H2SiO3↓
D. 成分为盐酸的洁厕灵与“84”消毒液混合使用易中毒:C1—+ C1O—+ 2H+=== Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确是( )
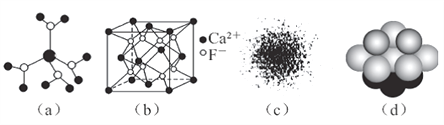
A. 水合铜离子的模型如图(a)所示,1个水合铜离子中有4个配位体
B. CaF2晶体的晶胞如图(b)所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图(c)所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图(d),为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应伴随着能量的变化.下列过程中的能量变化不是由化学反应引起的是( )
A.天然气燃烧
B.中和反应
C.冰的融化
D.Ba(OH)28H2O晶体与NH4Cl晶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月的eLife上发表了我国医学工作者的一篇论文。论文指出小苏打在治疗癌症的方法中功不可没。在实验室中制取NaHCO3的方法有多种。
方法一:模拟工业“侯氏制碱法”制取:(原理NaCl+H2O+CO2+NH3=NaHCO3↓+NH4Cl)
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:让某一装置先发生反应,直到产生的气体不能再在Ⅲ中溶解,再通入另一装置中产生的气体,片刻后,Ⅲ中出现固体。继续向Ⅲ中通入两种气体,直到不再有固体产生。
第三步:分离Ⅲ中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl固体粉末,有NH4Cl晶体析出。
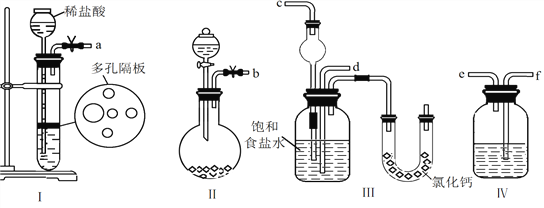 (1)图中所示装置的连接顺序是:a接f;e接________;b接________(填接口编号)。
(1)图中所示装置的连接顺序是:a接f;e接________;b接________(填接口编号)。
(2)Ⅰ中盛放稀盐酸的仪器名称是__________,Ⅱ中圆底烧瓶盛放试剂名称是__________,Ⅳ中应选用的液体为__________,实验室检验Ⅱ中生成气体的方法________________________。
(3)第二步中让__________(填序号)装置先发生反应。
(4)第四步中所得的晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,不使用其他任何试剂,证明所得晶体大部分是NH4C1。简要写出操作和现象_____________________________________。
方法二:把CO2通入饱和Na2CO3溶液制取NaHCO3。装置如下图所示(气密性已检验,部分夹持装置略):
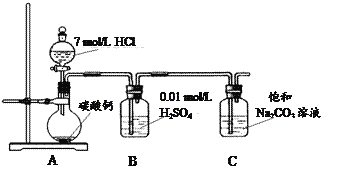
(5)装置B的作用之一是吸收挥发出来的HCl气体,另一作用可能为___________________(请结合化学平衡移动原理解释)
(6)NaHCO3溶液中含碳粒子浓度由大到小排序__________________________________
方法三:电解Na2CO3溶液也可生成NaHCO3,装置如图所示。
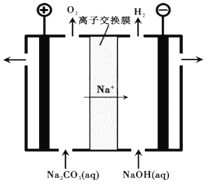
(7)①简述阳极液NaHCO3生成的原理:___________________________。
②产品NaHCO3中常混有Na2CO3,测试NaHCO3含量的方法是:准确称取样品Wg,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用c mol/L的标准盐酸溶液滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点),所用盐酸溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用盐酸溶液滴定至溶液由黄变橙,所用盐酸溶液体积为V2mL。写出产品中NaHCO3质量分数的计算式:______________用c、V1、V2、W表示);若配制标准液盐酸定容时俯视刻度线,则测得NaHCO3质量分数___________(填“偏大”“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去).请回答下列问题:

(1)水从冷凝管的______(填“a”或“b”)处进入。
(2)已知下列数据:
乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | ﹣ |
沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
又知温度高于140℃时发生副反应:2CH3CH2OH→CH3CH2OCH2CH3+H2O
①该副反应属于__________反应(填字母)。
a.加成 b.取代 c.酯化
②考虑到反应速率等多种因素,用上述装置制备乙酸乙酯时,反应的最佳温度范围是______(填字母)。
a.T<77.5℃ b.T>150℃ c.115℃<T<130℃
(3)上述实验中饱和碳酸钠溶液的作用是(填字母):___________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(4)欲分离出乙酸乙酯,应使用的分离方法是__________(填操作方法名称,下同),所用到的仪器为______ , 进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用____________的方法。
(5)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g,则乙酸乙酯的产率是_______。
(6)乙二酸和乙二醇也能发生酯化反应,写出生成环酯的化学反应方程式____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com