
| A£® | æÉÓĆĮĖ“ļ¶ūĻÖĻóĒų·ÖČÜŅŗÓė½ŗĢå | |
| B£® | ÉśŹÆ»ŅÓėĖ®»ģŗĻµÄ¹ż³ĢÖ»·¢ÉśĪļĄķ±ä»Æ | |
| C£® | Ć÷·Æ¾»Ė®Ö»·¢ÉśĮĖĪļĄķ±ä»Æ | |
| D£® | CuSO4•5H20 ŹĒŅ»ÖÖ»ģŗĻĪļ |
·ÖĪö A£®½ŗĢåÓŠ¶”“ļ¶ūŠ§Ó¦£¬ČÜŅŗƻӊ£»
B£®ÉśŹÆ»ŅŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬ŹōÓŚ»Æѧ±ä»Æ£»
C£®ĀĮĄė×ÓĖ®½āÉś³ÉĒāŃõ»ÆĀĮ½ŗĢåŗĶĒāĄė×Ó£»
D£®»ģŗĻĪļŹĒ²»Ķ¬ĪļÖŹ×é³ÉµÄĪļÖŹ£®
½ā“š ½ā£ŗA£®½ŗĢåÓŠ¶”“ļ¶ūŠ§Ó¦£¬ČÜŅŗƻӊ£¬¹ŹĄūÓƶ”“ļ¶ūŠ§Ó¦æÉŅŌĒų·ÖČÜŅŗŗĶ½ŗĢ壬¹ŹAÕżČ·£»
B£®ÉśŹÆ»ŅŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬·“Ó¦·½³ĢŹ½ĪŖCaO+H2O=Ca£ØOH£©2£¬øƱä»ÆŹōÓŚ»Æѧ±ä»Æ£¬¹ŹB“ķĪó£»
C£®ĀĮĄė×ÓĖ®½āÉś³ÉĒāŃõ»ÆĀĮ½ŗĢåŗĶĒāĄė×Ó£¬ĒāŃõ»ÆĀĮ½ŗĢå¾ßÓŠĪüø½ŠŌ£¬Īüø½Ė®ÖŠµÄŠüø”Īļ£¬ÓŠŠĀĪļÖŹÉś³É£¬ŹōÓŚ»Æѧ±ä»Æ£¬¹ŹC“ķĪó£»
D£®CuSO4•5H2OÖ»ŗ¬Ņ»ÖÖĪļÖŹ£¬ŹĒ“æ¾»Īļ£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éÄŚČŻ½Ļ¶ą£¬Éę¼°½ŗĢ唢»Æѧ±ä»Æ”¢ĪļÖŹµÄ·ÖĄąµČ£¬ĢāÄæÄŃ¶Č²»“ó£¬Ń§Ļ°ÖŠ×¢ŅāĻą¹Ų»ł“”ÖŖŹ¶µÄ»żĄŪ£®


 ÖÜÖÜĒå¼ģ²āĻµĮŠ“š°ø
ÖÜÖÜĒå¼ģ²āĻµĮŠ“š°ø ĒįĒɶį¹ŚÖܲāŌĀæ¼Ö±ĶØøßæ¼ĻµĮŠ“š°ø
ĒįĒɶį¹ŚÖܲāŌĀæ¼Ö±ĶØøßæ¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÄĘÓėĖ®·“Ó¦£ŗNa+2H2OØTNa++2OH-+H2”ü | |
| B£® | Ķ·ŪÓėĻ”ĻõĖįµÄ·“Ó¦£ŗCu+2H+ØTCu2++H2”ü | |
| C£® | ĒāŃõ»ÆĶÓėĻ”ŃĪĖį·“Ó¦£ŗOH-+H+ØTH2O | |
| D£® | Ģ¼ĖįÄĘČÜŅŗÓė×ćĮæĻ”ĮņĖįµÄ·“Ó¦£ŗCO32-+2H+ØTH2O+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«±½ÓėÅØĻõĖį”¢ÅØĮņĖįµÄ»ģŗĻĪļŌŚ100”ęĖ®Ō”¼ÓČČĢõ¼žĻĀ·“Ó¦æÉÉś³ÉĻõ»ł±½ | |
| B£® | ÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗ¼“æɼģŃéCH2ØTCH-CHOÖŠµÄĢ¼Ģ¼Ė«¼ü | |
| C£® | ½«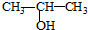 ÓėNaOHµÄ“¼ČÜŅŗ¹²ČČÖʱøCH3-CHØTCH2 ÓėNaOHµÄ“¼ČÜŅŗ¹²ČČÖʱøCH3-CHØTCH2 | |
| D£® | ĄūÓĆŗĖ“Ź²ÕńĒāĘ×£¬æÉŅŌ¼ų±šCH3OCH3ŗĶCH3CH2OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1LCO2ÖŠŗ¬ÓŠ3NAøöŌ×Ó | |
| B£® | 1molCl2ŗ¬ÓŠ1NAøöŌ×Ó | |
| C£® | 23gÄĘŌŚ×ćĮæµÄCl2ÖŠ·“Ó¦£¬×ŖŅʵē×ÓŹżNAøö | |
| D£® | ÓūÅäÖĘ1.00L1.00mol•L-1µÄNaClČÜŅŗ£¬æɽ«58.5gNaClČÜÓŚ1.00LĖ®ÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | ¼× | ŅŅ | ±ū |
| ¢Ł | CO2 | NO2 | Ca£ØOH£©2 |
| ¢Ś | HCl | CO2 | Ca£ØOH£©2 |
| ¢Ū | NO2 | NH3 | MgCl2 |
| ¢Ü | NO2 | O2 | BaCl2 |
| ¢Ż | CO2 | NH3 | CaCl2 |
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ł¢Ü¢Ż | C£® | ¢Ł¢Ś¢Ū¢Ż | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Al£ØOH£©3 | Fe£ØOH£©2 | Fe£ØOH£©3 | |
| æŖŹ¼³ĮµķŹ± | 3.4 | 6.3 | 1.5 |
| ĶźČ«³ĮµķŹ± | 4.7 | 8.3 | 2.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
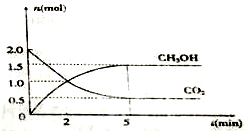 ”°µĶĢ¼Ń»·”±ŅżĘšĮĖČ«ŹĄ½ēµÄø߶ČÖŲŹÓ£¬¼õÅÅCO2µÄŅ»ÖÖ·½·ØŹĒ£ŗ
”°µĶĢ¼Ń»·”±ŅżĘšĮĖČ«ŹĄ½ēµÄø߶ČÖŲŹÓ£¬¼õÅÅCO2µÄŅ»ÖÖ·½·ØŹĒ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
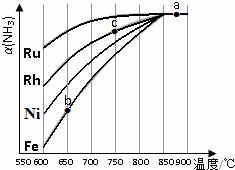 °±ĘųŌŚÉś²ś”¢Éś»īŗĶæĘŃŠÖŠÓ¦ÓĆŹ®·Ö¹ć·ŗ
°±ĘųŌŚÉś²ś”¢Éś»īŗĶæĘŃŠÖŠÓ¦ÓĆŹ®·Ö¹ć·ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com