
| 选项 | 实验事实 | 结论 |
| A | 其他条件不变,0.01mol•L-1的酸性KMnO4溶液分别与0.1mol•L-1的H2C2O4溶液和0.2mol•L-1的H2C2O4溶液反应,后者褪色时间短 | 当其他条件不变时,增大反应物浓度可以使化学反应速率加快 |
| B | 其他条件不变,分别将等体积、等物质的量浓度的Na2S2O3溶液和H2SO4混合液放在冷水和热水中,放在热水中的混合液先出现浑浊 | 当其他条件不变时,反应体系的温度越高,化学反应速率越快 |
| C | 将少量MnO2粉末加入盛有10%双氧水的锥形瓶内,在化学反应前后,MnO2的质量和化学性质都没有发生改变 | 催化剂虽然可以加快化学反应的速率,但一定不参与化学反应过程 |
| D | 一定条件下,分别在容积为1L和容积为2L的两个密闭容器中加入等量的氢气和碘蒸气,发生如下反应:H2(g)+I2(g)?2HI(g),获得等量HI时需要的时间前者少 | 当其他条件不变时,气态反应体系的压强越大,化学反应速率越快 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.浓度增大会加快反应速率;
B.温度变化一定对反应速率影响,升温,速率增大,降温反应速率减小;
C.催化剂改变化学反应速率,不改变化学平衡,催化剂在反应前后质量和化学性质不变,催化剂参与反应过程,降低活化能;
D.压强增大会增大化学反应速率.
解答 解:A.草酸浓度大,反应速率快,反应需要的时间短,浓度增大会加快反应速率,故A正确;
B.温度变化一定对反应速率影响,升温,速率增大,降温反应速率减小;Na2S2O3溶液和H2SO4混合液在热水中浑浊现象快,反应速率快,故B正确;
C.催化剂改变化学反应速率,不改变化学平衡,催化剂在反应前后质量和化学性质不变,催化剂参与反应过程,降低活化能,故C错误;
D.对有气体的反应,压强增大会增大化学反应速率,故D正确;
故选C.
点评 本题考查了化学反应速率的影响因素分析判断,为高频考点,侧重考查学生的分析能力,注意把握实验验证方法,掌握影响化学反应速率的影响因素和结果是解题关键,题目难度中等.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| B. | 已知C(s)+O2(g)═CO2(g)△H1 C(s)+$\frac{1}{2}$O2(g)=CO(g)△H2;则△H2>△H1 | |
| C. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol | |
| D. | 放热过程(△H<0)或熵增加(△S>0)的过程一定是自发的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Z |
| A. | 非金属性:W<Z | B. | 简单离子的半径:X2-<Y2+ | ||
| C. | 沸点:H2X<H2Z | D. | WX2的电子式为: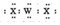 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S$→_{点燃}^{足量O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | SiO2$\stackrel{盐酸}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| C. | NH3$→_{催化剂、△}^{O_{2}}$NO$\stackrel{O_{2}}{→}$NO2 | |
| D. | Fe$→_{点燃}^{少量Cl_{2}}$FeCl2$\stackrel{NaOH溶液}{→}$Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
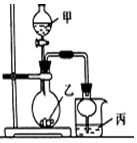 利用图所示装置进行下列实验,其中丙中实验现象描述正确的是( )
利用图所示装置进行下列实验,其中丙中实验现象描述正确的是( )| 实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
| A | 70%硫酸 | Na2SO3 | 紫色石蕊试液 | 溶液先变红后褪色 |
| B | 浓盐酸 | KMnO4 | 含酚酞的NaOH溶液 | 溶液褪色 |
| C | 稀盐酸 | CaCO3 | BaCl2溶液 | 有白色沉淀生成 |
| D | 浓氨水 | CaO | AlCl3溶液 | 先生成白色沉淀然后沉淀溶解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制七个基本物理量之一 | |
| B. | 1 L 0.1 mol/L BaCl2溶液中所含的Cl-为0.1 NA | |
| C. | 常温常压下,11.2 L Cl2所含的分子数为0.5 NA | |
| D. | 常温常压下,32 g O2含有的氧原子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气极易溶解于水且溶解的快,因此可用来做喷泉实验 | |
| B. | 实验室可用氢氧化钠溶液处理含有二氧化硫或氯气的尾气 | |
| C. | 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
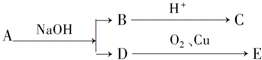
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com