
| A. | 标准状况下,1mol Cl2和HCl的混合气体所含分子总数为2NA | |
| B. | 101kPa、0℃时,22.4 L H2中氢原子数为NA个 | |
| C. | 标准状况下,2.24 L CCl4含有的碳原子数目为0.1NA | |
| D. | 常温常压下3.2 g O2中含有的氧原子数目为0.2 NA |
分析 A.依据标准状况n=$\frac{V}{22.4}$=$\frac{N}{{N}_{A}}$计算物质的量,得到分子数;
B.1个氢气分子含有2个氢原子;
C.气体摩尔体积适用对象为气体;
D.根据n=$\frac{m}{M}$并根据1molO2中含2mol氧原子来分析.
解答 解:A.依据标准状况n=$\frac{V}{22.4}$计算物质的量=$\frac{22.4L}{22.4L/mol}$=1mol,得到分子数 NA,故A错误;
B.101kPa、0℃时,22.4 L H2的物质的量为1mol,含有氢原子物质的量为2mol,个数为2NA个,故B错误;
C.标况下,四氯化碳为液体,不能使用气体摩尔体积,故C错误;
D.3.2 g O2的物质的量n=$\frac{m}{M}$=$\frac{3.2g}{32g/mol}$=0.1mol,而1molO2中含2mol氧原子,故0.1mol氧气中含0.2mol氧原子,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意物质的组成、结构,注意气体摩尔体积使用条件和对象,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 将一小块钠投入到盛有硫酸铜溶液的烧杯中,发现没有紫红色的铜析出,不能说明钠的金属性比铜弱 | |
| B. | 用湿润的淀粉碘化钾试纸放置在有氯气产生的导管上端,发现试纸变蓝,说明氯元素的非金属性比碘元素强 | |
| C. | 把H2S气体和Cl2在集气瓶中混合,一段时间后发现瓶壁有淡黄色固体析出,说明Cl的非金属性比S强 | |
| D. | 将0.1 mol Na、Mg、Al分别与足量稀盐酸反应,金属失去的电子数分别为0.1 mol、0.2 mol、0.3 mol,说明这三种金属的活泼性为:Al>Mg>Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池是把电能转化为化学能的装置 | |
| B. | 原电池中电子流出的一极是负极,发生还原反应 | |
| C. | 构成原电池的两极必须是两种不同的金属 | |
| D. | Cu-Fe稀硫酸原电池工作时,铜是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 盐酸的浓度(mol?L-1) | MOH溶液的浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | 0.2 | c1 | 7 |
| 丙 | 0.1 | 0.1 | 5 |
| A. | 甲组混合溶液中M+水解程度较丙组中大,且a<5 | |
| B. | 甲组混合溶液中:c(Cl-)>c(M+)>c(H+)>c(OH-) | |
| C. | 乙组混合溶液中:c(M+)+c(MOH)>0.1mol?L-1,且c1>0.2 | |
| D. | 丙组混合溶液中:c(OH-)+c(MOH)=1×10-5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2+H2O═HCl+HClO | B. | 3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 3NO2+H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
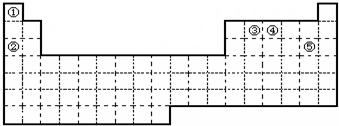
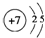 ,
,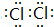 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com