
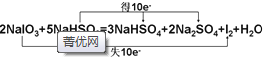
 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
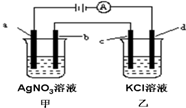 如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )| A、乙烧杯中的d电极反应式为Fe-2e-=Fe2+ |
| B、当电解一段时间后,将甲、乙两溶液混合,一定会沉淀 |
| C、当b极增重5.4g时,d极产生的气体为2.24L(标准状况) |
| D、甲烧杯中溶液的pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性:SO2可以被Cr2O72-氧化 |
| B、还原性:Cr3+>Fe2+>SO2 |
| C、Cr2O72-在反应中做还原剂 |
| D、两个反应中Fe3+均表现还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该元素位于第五周期IB族 |
| B、该元素原子核外有5个电子层 |
| C、该元素原子最外层共有2个电子 |
| D、该元素原子M层上共有18个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1?min-1 |
| B、0.2mol?L-1?min-1 |
| C、0.9mol?L-1?min-1 |
| D、1.0mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、3O2
| ||||
| B、Cu+2FeCl3═CuCl2+2FeCl2 | ||||
C、2Al+Fe2O3
| ||||
| D、2H2O2═2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、15% | B、<15% |
| C、>15% | D、30% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将22.4 L HCl气体溶于水稀释至200 mL |
| B、将36.5 g HCl气体溶于200 mL水中 |
| C、取10 mol/L的盐酸100 mL加水100 mL |
| D、取10 mol/L的盐酸100 mL加水稀释至200 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com