
| A.混合溶液的pH等于7 | B.混合溶液的pH大于7 |
| C.加入酸碱的物质的量相等 | D.混合溶液还能再中和盐酸 |
科目:高中化学 来源:不详 题型:单选题
| A.α1<α2<α3<α4 | B.α3=α2<α1<α4 |
| C.α2<α3<α1<α4 | D.α2=α3<α4<α1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:9 | B.1:1 | C.2:9 | D.1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1×10-7mol·L-1 | B.1×10-12mol·L-1 |
| C.1×10-2mol·L-1 | D.1×10-14mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.水的电离常数KW数值大小关系为:b>c>d |
| B.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| C.温度不变,加入少量NaOH可使溶液从c点变到 a点 |
| D.在b点对应温度下,将pH=2的HCl与pH=10的NaOH溶液等体积混合后,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2O的电子式为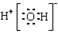 |
| B.273K、101kPa,水的分子间距离:d(气态)>d(液态)>d(固态) |
| C.4℃时,纯水的pH=7 |
| D.D216O中,质量数之和是质子数之和的两倍 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.10mol·L-1的三种溶液:①NaCl、②NaOH、③CH3COONa,其pH大小顺序为:③>②>① |
| B.0.10mol·L-1NaHCO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=0.10mol·L-1 |
| C.pH=2的盐酸和pH=12的NaOH溶液中,水的离子积Kw相同 |
| D.与体积相同、pH=2的盐酸和醋酸完全反应,需要0.010mol·L-1 NaOH的体积相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入指示剂。 |
| B.用待测定的溶液润洗酸式滴定管。 |
| C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com