
| A、氯气用于自来水杀菌消毒 |
| B、晶体硅用于制造光导纤维 |
| C、氨用于制备硝酸 |
| D、氧化铁用于制造红色涂料 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、所有烷烃和糖类中都存在碳碳单键 |
| B、丁烷有两种同分异构体 |
| C、甲烷与氯气混合光照后黄绿色消失,是因为发生了加成反应 |
| D、向蛋白质溶液中加入饱和食盐水,蛋白质析出,加水也不溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、改变条件,反应物的转化率增大,平衡常数也一定增大 | ||||||
| B、反应2NO2(g)═N2O4(g)△H<0,升高温度该反应平衡常数增大 | ||||||
| C、对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等 | ||||||
D、CO2+H2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、催化剂能使不起反应的物质发生反应 |
| B、在化学反应前后催化剂性质和质量都发生改变 |
| C、催化剂能改变化学反应速率 |
| D、在化学反应过程中,一定不参与化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
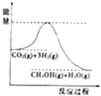 一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:
一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com