
【题目】下列说法正确的是( )
A.醋酸钠溶液呈碱性,往0.1mol·L-1醋酸溶液加入少量醋酸钠固体后,可促进醋酸电离
B.T℃时,pH为6.8的溶液,该溶液一定呈酸性
C.相同温度下,pH相等的氨水、NaOH溶液中,n(NH4+)与n(Na+)相等
D.pH相等的盐酸和醋酸溶液等体积混合(忽略温度和体积变化),混合溶液中c(Cl-) = c(CH3COO-)
【答案】D
【解析】
A.醋酸的电离平衡为:CH3COOH![]() CH3COO-+H+,加入醋酸钠固体,CH3COO-浓度增大,醋酸电离平衡逆向移动,抑制醋酸电离,A错误;
CH3COO-+H+,加入醋酸钠固体,CH3COO-浓度增大,醋酸电离平衡逆向移动,抑制醋酸电离,A错误;
B.判断溶液的酸碱性,要通过比较H+和OH-浓度的相对大小来判断,不能单从pH角度来判断溶液的酸碱性,B错误;
C.没有给溶液的体积,无法判断n(NH4+)与n(Na+)是否相等,C错误;
D.两种溶液的pH相等,则混合前两种溶液中c(H+)和c(OH-)分别相等,因为是等体积混合,所以混合后溶液中c(H+)和c(OH-)和混合前相等。HCl溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(H+),混合后存在电荷守恒:c混(Cl-)+c混(OH-)+c混(CH3COO-)=c混(H+),所以c(Cl-)= c混(Cl-)+c混(CH3COO-),又因为是等体积混合,有c混(Cl-)=![]() c(Cl-),所以,c混(CH3COO-)= c(Cl-)-
c(Cl-),所以,c混(CH3COO-)= c(Cl-)-![]() c(Cl-)=
c(Cl-)=![]() c(Cl-),综上所述:c混(Cl-)= c混(CH3COO-),即pH相等的盐酸和醋酸溶液等体积混合(忽略温度和体积变化),混合溶液中c(Cl-) = c(CH3COO-),D正确。
c(Cl-),综上所述:c混(Cl-)= c混(CH3COO-),即pH相等的盐酸和醋酸溶液等体积混合(忽略温度和体积变化),混合溶液中c(Cl-) = c(CH3COO-),D正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】某医药中间体F的制备流程如图(部分产物已略去)。
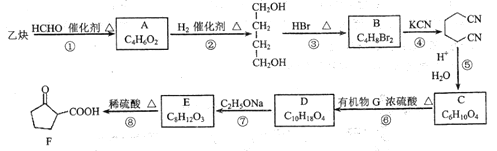
已知: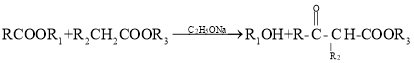 (
(![]() 表示烃基)
表示烃基)
(1)F中含有官能团的名称是羧基和_______。
(2)实验室制取乙炔的化学方程式为____________。
(3)A不能发生银镜反应,则A的结构简式为_________。
(4)反应①~④中,属于加成反应的是___________(填序号)。
(5)反应⑥的化学方程式为________。
(6)E的结构简式为________。
(7)某聚合物![]() 的单体与
的单体与![]() 互为同分异构体,该单体核磁共振氢谱有三个峰,峰面积之比为
互为同分异构体,该单体核磁共振氢谱有三个峰,峰面积之比为![]() ,且能与
,且能与![]() 溶液反应,则聚合物
溶液反应,则聚合物![]() 的结构简式是_______。
的结构简式是_______。
(8)已知:i. ![]() +
+![]()
![]()
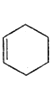
ii.RCH=CHR′![]() RCHO+R′CHO(R,R′表示烃基)
RCHO+R′CHO(R,R′表示烃基)
以![]() 和
和![]() 为起始原料合成
为起始原料合成![]() ,选用必要的无机试剂,写出合成路线流程图: _______________。合成路流程图例:
,选用必要的无机试剂,写出合成路线流程图: _______________。合成路流程图例:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2NO(g) + 2CO(g)![]() N2(g) + 2CO2(g) ΔH<0可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO 和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法不正确的是
N2(g) + 2CO2(g) ΔH<0可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO 和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法不正确的是
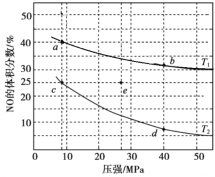
A.温度:T1>T2
B.a点达到平衡所需时间比c点短
C.c点NO的平衡转化率:50%
D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】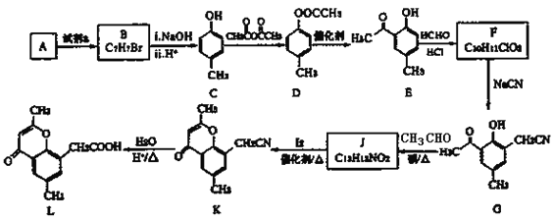
已知:①R-X![]() R-CN
R-CN![]() R-COOH
R-COOH
②R1CHO+CH3COR2![]() R1CH=CHCOR2
R1CH=CHCOR2
③![]()
(1)A 的分子式是 C7H8,写出 A→B 反应的化学方程式_____。
(2)写出 C→D 的化学方程式_____。
(3)E 与 HCHO 反应的反应类型为_____,写出 F 的结构简式_____。
(4)写出 D 与足量 NaOH 溶液反应的化学方程式____________。
(5)写出 J 与 I2 反应生成 K 和 HI 的化学方程式____________________。
(6)以 A 和乙烯为起始原料,结合题中信息,选用必要的无机试剂合成苯乙酸乙酯(![]() ),写出相应的合成路线_____________。
),写出相应的合成路线_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.乙醛和乙烯均能使溴水褪色,两者的反应原理不同
B.淀粉和纤维素均可以制酒精,酒精在某种微生物作用下发生氧化反应得到醋酸
C.蛋白质溶液在强酸、强碱、紫外线和加热条件下都能发生变性
D.甲苯的一氯代物有4种,甲苯与氢气加成后的产物的一氯代物也只有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W为常见的主族元素,根据下表信息回答问题:
元素 | 元素性质或原子结构信息 |
X | 短周期元素原子半径最大(稀有气体元素不参与比较) |
Y | +3价阳离子的核外电子排布与氖原子相同 |
Z | 原子核外M电子层与K电子层的电子数相等 |
R | 与Z同周期,主要化合价为1、+7 |
W | 原子结构示意图: |
(1)写出元素X的原子结构示意图_____;元素W在周期表中位置_____。
(2)Y、Z最高价氧化物对应水化物的碱性强弱比较_____>_____(填化学式)。
(3)用电子式表示X和R形成化合物的过程:_____。
(4)下列对于W及其化合物的推断中,正确的是_____(填序号)。
①W的最低负化合价与R的最低负化合价相同
②W的氢化物的稳定性弱于R的氢化物的稳定性
③W的单质可与X和R形成的化合物的水溶液发生置换反应
④W的最高价氧化物对应水化物的酸性比R的强
(5)为验证卤族部分元素单质氧化性的递变规律,设计如图装置进行实验,请回答:

①A中发生的反应的离子方程式是_____。
②棉花中浸有的NaOH溶液的作用是_____(用离子方程式表示)。
③为验证Br2与I2的氧化性强弱:通入一定量R的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到_____。该实验必须控制加入的R单质的量,否则得不出Br2的氧化性比I2强。理由是______。
④从原子结构的角度解释卤族元素单质氧化性逐渐减弱的原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )

A. 所含原子数相等 B. 气体密度相等C.气体质量相等 D.摩尔质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为验证同主族元素非金属性的变化规律,设计了如下实验(实验装置如图所示)。
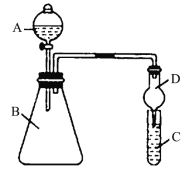
(1)仪器A的名称为___,干燥管D的作用是___。
(2)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为___。
(3)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4固体,C中加淀粉碘化钾混合溶液,观察到___,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用___溶液吸收尾气。
(4)课外活动小组在A中加盐酸、B中加CaCO3固体,C中加Na2SiO3溶液,观察到C中产生白色沉淀(H2SiO3),请你利用原子结构知识解释这一现象:___;有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加盛有___的洗气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动汽车已逐渐走入人们的生活,一些电动汽车动力使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A极材料是金属锂和石墨的复合材料(石墨作为金属锂的载体),电解质为一种能传导Li+的高分子材料。隔膜只允许特定的离子通过,电池反应式为LixC6+Li1xCoO2![]() C6+LiCoO2,下列说法不正确的是
C6+LiCoO2,下列说法不正确的是

A. 该隔膜只允许Li+通过,放电时Li+从左边移向右边
B. 充电时,B电极与电源正极相连
C. 电池放电时,负极的电极反应式为LixC6xe![]() xLi++C6
xLi++C6
D. 废旧钴酸锂电池进行“放电处理”让Li+进入石墨中而有利于回收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com